
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
Психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Контрольная работа: Классы неорганических веществ. Растворы электролитов. Размеры атомов и водородная связь
Контрольная работа: Классы неорганических веществ. Растворы электролитов. Размеры атомов и водородная связь
Содержание
1. Классы неорганических веществ
2. Размеры атомов. Связь размера атома с положением в периодической системе элементов. Понятие об ионах
3. Водородная связь
4. Энтальпия
5. Растворы электролитов. Понятие об электролитической диссоциации
6. Мембранные сенсоры и биосенсоры
7. Литература
1. Классы неорганических веществ
Классификация неорганических веществ прошла долгий путь развития и складывалась постепенно, начиная с первых опытов алхимиков.
Химические элементы делятся на элементы с металлическими и неметаллическими свойствами.
Многие элементы в соответствии с Периодическим законом проявляют одновременно в той или иной мере свойства металлов и неметаллов. Такие элементы называют амфотерными.
В силу большого своеобразия химических свойств особо выделяют благородные газы - элементы VIII A-группы.
Соответственно подразделению элементов классифицируют простые (одноэлементные) вещества - формы существования элементов в свободном виде.
Классификация сложных веществ (двух- или многоэлементных веществ) по составу основана на наличии в соединении самого распространенного в природе элемента кислорода и на самом распространенном соединении кислорода - воде.
Кислород образует соединения со всеми элементами, кроме He, Ne и Ar. Среди производных кислорода только соединения со фтором (например дифторид кислорода OF2) содержат кислород в положительной степени окисления; практически все остальные соединения кислорода - это оксиды.
При реакции оксидов с водой (напрямую или косвенным путем) получаются гидроксиды - кислотные, основные или амфотерные.
Гидроксиды разных типов реагируют между собой и образуют кислородсодержащие соли, состоящие из катионов и анионов (кислотных остатков). Такие соли называют средними. Если соли содержат два химически разных катиона или два разных кислотных остатка, их называют соответственно двойными и смешанными.
При наличии в составе кислотного остатка атомов водорода, способных к дальнейшему замещению катионами, соли называются кислыми, при наличии гидроксогрупп OH− (или оксогрупп O2−) - основными солями.
Еще один обширный класс сложных веществ - бинарные соединения.
2. Размеры атомов. Связь размера атома с положением в периодической системе элементов. Понятие об ионах
Атом состоит из положительно заряженного ядра и вращающихся вокруг него отрицательно заряженных частиц‑электронов, составляющих его электронную оболочку. Сумма зарядов электронов равна по модулю положительному заряду ядра, поэтому атом в целом представляет собой электронейтральную систему. Размеры атома определяются размерами его электронной оболочки и составляют величину порядка 10–8 см.
Массы различных элементов находятся в пределах от 1,6×10–24 до 4×10–22 г.
В ядерной физике масса, заряд и энергия измеряются специальными единицами. Масса измеряется в атомных единицах массы (а.е.м.). За атомную единицу принята 1/12 массы атома углерода, равная 1,66057×10–30 г. Элементарным называется заряд, который равен по абсолютной величине заряду электрона: 1 е =1,601×10‑19 Кал = 4,802×10‑10 в единицах CГСE. Энергия измеряется в электрон-вольтах (эВ). Электрон‑вольт соответствует энергии, которую приобретает электрон при движении в электрическом поле с разностью потенциалов в 1В (Вольт): 1эВ = 3,8276 ×10‑20 кал (калорий). В ядерной физике часто применяется единица, в миллион раз большая:
МэВ = 106 эВ = 1,602×10‑6 эрг = 3,83×10‑14 кал = 1,60219·10‑13 Дж.
Электроны в оболочке атома расположены слоями. Число электронных слоев равно порядковому номеру химического элемента в периодической системе элементов Д.И. Менделеева.
В первом, ближайшем к ядру слое К вращается не более двух электронов. В следующем за ним слое L – не более 8, в слое М – не более 18, а в четвертом слое N – не более 32 электронов. Таким образом, наибольшее число электронов этих слоев равно удвоенному квадрату номера слоя Z = 2n2. В последующих слоях это правило нарушается, и количество электронов может составлять: в пятом слое О – от 1 до 29, в шестом слое Р – от 1 до 9 и в дополнительном (последнем) слое Q – не более 2 электронов.
Каждый атом существует лишь в определенных дискретных энергетических состояниях, соответствующих строго определенному значению его энергии.
Переход атома из одного энергетического состояния в другое сопровождается поглощением или излучением энергии. В обычном же состоянии атом не излучает.
Если одному из электронов при столкновении с какой-либо частицей извне будет сообщена некоторая дополнительная энергия, то он перейдет на более удаленную орбиту того слоя, которому соответствует его новая энергия. В этом случае атом приходит в возбужденное состояние, и тогда один из электронов внешнего слоя перескакивает на освободившееся место. Через короткое время (порядка 10‑8 с) атом возвращается в нормальное состояние, испуская при этом видимый свет, ультрафиолетовое или рентгеновское излучение.
Ион (греч. ιоν — «идущий») — электрически заряженная частица (атом, молекула), образующаяся, обычно, в результате потери или присоединения одного или нескольких электронов атомами или молекулами.
Заряд иона кратен заряду электрона. Понятие и термин ион ввёл в 1834 Майкл Фарадей, который, изучая действие электрического тока на водные растворы кислот, щелочей и солей, предположил, что электропроводность таких растворов обусловлена движением ионов. Положительно заряженные ионы, движущиеся в растворе к отрицательному полюсу (катоду), Фарадей назвал катионами, а отрицательно заряженные, движущиеся к положительному полюсу (аноду) — анионами.
В виде самостоятельных частиц они встречаются во всех агрегатных состояниях вещества — в газах (в частности, в атмосфере), в жидкостях (в расплавах и в растворах), в кристаллах и в плазме (в частности в межзвёздном пространстве).
Являясь химически активными частицами, ионы вступают в реакции с атомами, молекулами и между собой. В растворах ионы образуются в результате электролитической диссоциации и обусловливают свойства электролитов.
3. Водородная связь
Водородная связь — разновидность невалентного взаимодействия между атомом водорода H, ковалентно связанным с атомом A группы A-H молекулы RA-H и электроотрицательным атомом B другой молекулы (или функциональной группы той же молекулы) BR. Результатом таких взаимодействий являются комплексы RA-H•••BR различной степени стабильности, в которых атом водорода выступает в роли мостика, связывающего фрагменты RA и BR. Атом водорода, соединенный с атомом сильно электроотрицательного элемента, способен к образованию еще одной химической связи с подобным атомом водорода. Эта связь называется водородной. Возникновение водородной связи можно в первом приближении объяснить действием электростатических сил. Атом с большой электроотрицательностью, например, фтор в молекуле HF смещает на себя электронное облако, приобретая значительный эффективный отрицательный заряд, а ядро атома водорода (протон) почти лишается электронного облака и приобретает эффективный положительный заряд. Между протоном атома водорода и отрицательно заряженным атомом фтора соседней молекулы возникает электростатическое притяжение, что и приводит к образованию водородной связи. Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, т.е. их объединение в димеры или полимеры. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак. Водородная связь в значительной мере определяет свойства и таких биологически важных веществ как белки и нуклеиновые кислоты.
4. Энтальпия
Энтальпиия, также тепловая функция и теплосодержание — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц.
Если термомеханическую систему рассматривать как состоящую из макротела (газа) и поршня с грузом Р = p S, уравновешивающего давление газа р внутри сосуда, то такая система называется расширенной.
Энтальпия или энергия расширенной системы Е равна сумме внутренней энергии газа U и потенциальной энергии поршня с грузом
Eпот = pSx = pV
H = E = U + pV
Таким образом, энтальпия в данном состоянии представляет собой сумму внутренней энергии тела и работы, которую необходимо затратить, чтобы тело объёмом V ввести в окружающую среду, имеющую давление р и находящуюся с телом в равновесном состоянии. Энтальпия системы H — аналогично внутренней энергии — имеет вполне определенное значение для каждого состояния, т. е. является функцией состояния. Следовательно, в процессе изменения состояния
ΔH = H2 − H1
Энтальпией системы удобно пользоваться в тех случаях, когда в качестве независимых переменных, определяющих состояние системы, выбирают давление р и температуру Т
H = H(p,T)
Энтальпия — величина аддитивная, т. е. для сложной системы равна сумме энтальпий её независимых частей
![]() .
.
Энтальпия определяется с точностью до постоянного слагаемого, которому в термодинамике часто придают произвольные значения (например, при расчете и построении тепловых диаграмм). При наличии немеханических сил величина энтальпии системы равна
![]()
где Xi — обобщённая сила; yi — обобщённая координата.
Изменение энтальпии не зависит от пути процесса, так как изменение объёма при постоянном давлении определяется только начальным и конечным состоянием системы. Если система каким-либо путём возвращается в исходное состояние (круговой процесс), то изменение любого её параметра равно нулю, а отсюда ΔU = 0 и ΔH = 0.
5. Растворы электролитов. Понятие об электролитической диссоциации
Электролиты. Известно, что существуют две основные причины прохождения электрического тока через проводники: либо за счет движения электронов в электрическом поле, либо за счет движения ионов. Электронная проводимость присуща, прежде всего, металлам.
Ионная проводимость присуща многим химическим соединениям, обладающим ионным строением, например солям в твердом или расплавленном состояниях, а также многим водным и неводным растворам. В связи с этим все вещества принято условно делить по их поведению в растворах на две категории: а) вещества, растворы которых обладают ионной проводимостью (электролиты); б) вещества, растворы которых не обладают ионной проводимостью (неэлектролиты). К электролитам относится большинство неорганических кислот, оснований и солей. К неэлектролитам относятся многие органические соединения, например спирты, углеводы.
Электролитическая диссоциация. Кроме хорошей электропроводности, растворы электролитов обладают более низкими значениями давления пара растворителя и температуры плавления и более высокими температурами кипения по сравнению с соответствующими значениями для чистого растворителя или для раствора неэлектролита в этом же растворителе. Для объяснения этих свойств, шведский ученый С. Аррениус в 1887 г. предложил теорию электролитической диссоциации.
Под электролитической диссоциацией понимается распад молекул электролита в растворе с образованием положительно и отрицательно заряженных ионов — катионов и анионов.
Процесс диссоциации во всех случаях является обратимым, поэтому при написании уравнений реакции диссоциации необходимо применять знак обратимости. Различные электролиты, согласно теории Аррениуса, диссоциируют на ионы в различной степени. Полнота распада зависит от природы электролита, его концентрации, природы растворителя, температуры. Степень диссоциации. Одним из важнейших понятий теории электролитической диссоциации Аррениуса является понятие о степени диссоциации. Степенью диссоциации а называется отношение числа молекул, распавшихся на ионы (n'), к общему числу растворенных молекул (n):
![]()
Из этого выражения очевидно, что а может изменяться от 0 (диссоциации нет) до 1 (полная диссоциация). Степень диссоциации часто выражают в процентах. Степень диссоциации электролита может быть определена только экспериментальным путем, например по измерению температуры замерзания раствора, по электропроводности раствора и т. д.
6. Мембранные сенсоры и биосенсоры
Электрохимические сенсоры и биосенсоры, устройства, в которых аналитический сигнал обеспечивается протеканием электрохимического процесса. Предназначены для качественного и количественного анализа химических соединений в жидких и газообразных средах. По сравнению с обычными аналитическими приборами отличаются портативностью, простотой конструкции, относительно низкой стоимостью. Электрохимические сенсоры составляют наиболее разработанную и широко используемую группу среди устройств, в которых аналитический сигнал обусловлен химическим взаимодействием в анализируемой среде. Различают потенциометрические, амперометрические, кондуктометрические, импедансометрические электрохимические сенсоры. Аналитическими сигналами служат, соотв.: потенциал индикаторного электрода (при нулевом токе через электрохимическую ячейку); ток, протекающий через ячейку при заданном значении электродного потенциала; электропроводность раствора электролита; электрохимический импеданс системы, представляющий собой электрический эквивалент определенного сочетания сопротивлений и емкостей в электрохимической цепи.
Электрохимические сенсоры используют главным образом для определения реакционноспособных (электроактивных) веществ, способных электрохимически восстанавливаться или окисляться на индикаторном электроде миниатюрной электрохимической ячейки, которая генерирует аналитический сигнал. В качестве индикаторных электродов служат инертные электроды (Pt, Pd, Au, Ag), химически активные (Сu, In, Sn) или модифицированные комплексные соединения, а также ионселективные электроды. Электролиты могут быть жидкими (растворы КС1, H2SO4, буферные растворы), твердыми (ZrO2, А12О3, Sb2O5 * nH2O), загущенными; применяют также полиэлектролиты.
В современных электрохимических сенсорах чувствительный элемент (трансдьюсер) по своей сути представляет гальванический элемент, предложенный Л. Кларком (1953), в котором два электрода и раствор электролита отделены от анализируемой среды полупроницаемой мембраной.
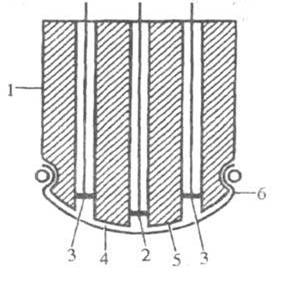
Рис. 1. Полярографический электрохимический детектор кислорода.
Например, в кислородном амперометрическом сенсоре (рис. 1) внутри цилиндрического корпуса 1 расположены индикаторный электрод 2 из платины и анод 3 из хлорида серебра (он же электрод сравнения). Электролит (водный раствор КС1) заливается в резервуар 4 и образует пленку 5 толщиной около 10 мкм. Полимерная мембрана 6 (полиэтилен, полипропилен, фторопласт, целлофан и др.) отделяет электролит от анализируемой среды (вода, газ), из которой кислород диффундирует через мембрану внутрь элемента и восстанавливается на катодно-поляризованном индикаторном электроде (реакция О2 + 4е- + 4Н+ = 2H2O). Ток восстановления определяется скоростью диффузии О2 сквозь мембрану. Скорость, в свою очередь, зависит от толщины и проницаемости мембраны. Катодная поляризация индикаторного электрода осуществляется как от постороннего источника тока, так и с помощью растворимого анода (гальванические сенсоры). Информативным параметром является предельный диффузионный ток при постоянном потенциале индикаторного электрода. Такие электрохимические сенсоры имеют, как правило, линейную зависимость электрического сигнала от парциального давления О2 (или др. электроактивного газа), что обеспечивает более высокую точность определения по сравнению, например, с потенциометрическим электрохимическим сенсором, в котором информативный параметр - равновесный (или квазиравновесный) электродный потенциал - имеет логарифмическую зависимость от содержания газа. Селективность электрохимических сенсоров определяется выбором подходящего материала электрода и рабочей области потенциалов. При анализе смеси газов необходимо, чтобы электрохимические реакции посторонних компонентов либо не имели места на данном электроде, либо протекали в области более высоких потенциалов.
Электрохимические сенсоры позволяют проводить анализ газообразных и жидких сред, в т. ч. суспензий, на содержание О2, О3, Н2, С12, H2S, оксидов N, С, S, причем без всякой пробоподготовки. Возможно определение концентраций, как больших (в случае выбросов, утечек загрязняющих газов и т. д.), так и малых - при контроле ПДК. Основные эксплуатационные характеристики электрохимических сенсоров: диапазон концентраций, чувствительность, селективность, быстродействие (время установления 90%-ного уровня сигнала), ресурс работы, отношение сигнал/шум. Диапазон концентраций Н2 и O2 составляет от 0 до 100% по объему, С12, SO2, H2S, CO - от 0,2 до 200 мг/м3 при быстродействии от 1 до 30 с. Отдельно выделяют электрохимические сенсоры для анализа биологических сред (биосенсоры). На индикаторном электроде биосенсоров закрепляется мембрана из целлофана с иммобилизованным ферментом (глюкозооксидаза, тирозиназа, фенолоксидаза, лакказа и др.). Определяют вещества, которые изменяют скорость ферментативных реакций: субстраты, ингибиторы, сами ферменты. Биосенсоры позволяют с высокой селективностью проводить автоматизированный анализ многокомпонентных систем на глюкозу, холестерин, мочевину, мочевую кислоту, аминокислоты и др. вещества, содержание которых варьирует от 0,05 мкг/мл до 1 мг/мл. Налажен промышленный выпуск электрохимических сенсоров для контроля содержания глюкозы в крови.
Перспективна разработка иммуноэлектрохимических сенсоров, в которых электрический сигнал преобразуется специфическим взаимодействием антиген - антитело.
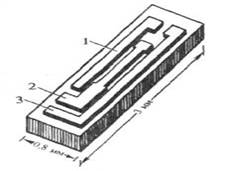
Рис. 2. Схема электрохимического сенсора, изготовленного методом фотолитографии.
Перспективным для серийного производства электрохимических сенсоров считается формирование электродного узла чувствительного элемента с использованием микроэлектронных технологий. На рис. 2 показан единичный чип, полученный методом фотолитографии. На кремниевой пластине длиной 3 мм, шириной 0,8 мм и толщиной 0,38 мм размещена трехэлектродная электрохимическая система: индикаторный электрод из Pt (1), вспомогательный электрод из Pt (2) и хлорсеребряный электрод сравнения (3).
7. Литература
1. Богдановская В. А. [и др.], в кн.: Итоги науки и техники, сер. Электрохимия, т. 31, М., 1990
2. Измайлов Н. А., Электрохимия растворов, 3 изд., М., 1976.
3. Общая и неорганическая химия. Т.1. Теоретические основы химии: Учебник для вузов в 2 томах. Под ред. А.Ф. Воробьева. – М.: ИКЦ "Академкнига", 2004. – 371 с.: ил.
4. Тарасевич М. Р. [и др.], в кн.: Итоги науки и техники, сер. Электрохимия, т. 35, М., 1992.
5. Цивадзе А.Ю., Воробьев А.Ф., Савинкина Е.В. и др. Неорганическая химия. 1 и 2 часть. - М., "Наука", 2004.
6. http://ru.wikipedia.org