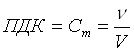Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
Психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Дипломная работа: Методика решения задач по теоретическим основам химической технологии
Дипломная работа: Методика решения задач по теоретическим основам химической технологии
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
Пензенский государственный педагогический университет
им. В.Г. Белинского
Факультет Кафедра
Естественно-географический Химии и теории и методики преподавания химии
ДИПЛОМНАЯ РАБОТА
"МЕТОДИКА РЕШЕНИЯ ЗАДАЧ ПО ТЕОРЕТИЧЕСКИМ ОСНОВАМ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ"
Пенза, 2007 г.
Содержание
Введение
1. Обзор литературы
1.1 Предмет химической технологии
1.2 Трактовка понятия «задача»
1.3 Значение химической задачи в процессе обучения
1.4 Требования к изучению химической задачи и ее место в процессе обучения
1.5 Система химических задач
1.6 Этапы решения задач
1.7 Классификация химических задач
2. Исследование трудностей, возникающих при решении задач теоретическим основам химической технологии
3. Методика решения задач по теоретическим основам химической технологии
3.1 Общие вопросы химической технологии
3.1.1 Термохимия
3.1.2 Химическое равновесие
3.1.3 Химическая кинетика
3.2 Технико-экономические показатели химических производств
3.3 Задачи с экологическим содержанием
3.4 Производство неорганических соединений
3.4.1 Металлургия
3.4.2 Электрохимические производства
3.5 Производство органических соединений
3.6 Творческие и изобретательские задачи
Выводы
Литература
Введение
Проблема методики решения задач в любой науке стоит достаточно остро, т.к. тщательная ее разработанность предполагает лучшую усвояемость научных знаний, их систематизированность и способность к применению в новых нестандартных ситуациях.
Дисциплина «Прикладная химия», целью которой является изучение производства и применения практически важных химических продуктов, базируется на принципах химической технологии. В настоящее время новые технологические процессы и системы управления ими создаются не эмпирически, а на основании рационального научного подхода, поэтому одним из разделов дисциплины «Прикладная химия» является «Теоретические основы химической технологии».
Изучение принципов химической технологии невозможно без количественных расчетов. Студент – будущий учитель химии, должен понимать, каким образом теоретические положения химии используются в промышленных процессах и повседневной жизни. Важной составляющей такого понимания является химическое мышление в целом и умение решать химические задачи, в частности.
Необходимо отметить специфику задач по химической технологии в рамках дисциплины «Прикладная химия». Как правило, это сложные, комплексные задачи, где требуются не только умения вести расчеты по уравнению химических реакций (часто многостадийные процессы), но и знания по разделам физической химии (термодинамика, кинетика, электрохимия), математики и физики. Поэтому не случайно изучение прикладной химии проходит именно на 5 курсе. Дисциплина «Прикладная химия» – это курс повторения, обобщения, систематизации химических знаний.
Целью дипломной работы было разработать методику решения задач по химической технологии в рамках изучения дисциплины «Прикладная химия».
Для достижения цели, нами поставлены следующие задачи:
1. Определить тематику задач дисциплины «Прикладная химия» в рамках раздела «Теоретические основы химической технологии».
2. Подобрать и составить задачи по выбранным темам.
3. Выявить основные трудности при решении задач по прикладной химии в рамках раздела «Теоретические основы химической технологии».
4. Разработать методику решения типовых задач.
Практической значимостью работы является возможность использования задач на занятиях по прикладной химии, для проведения коллоквиумов, индивидуального собеседования при защите лабораторных работ. Задачи по теоретическим аспектам химической технологии будут полезны и для учителей средней общеобразовательной школе при разработке элективных курсов. Общеизвестно, что овладение методикой обучения школьников решать задачи – одно из сложных профессиональных умений учителя.
1. Обзор литературы
1.1 Предмет химической технологии
Химическая технология является одной их основных химических дисциплин в педагогическом вузе. Она призвана дать студентам систему знаний о современном химическом производстве, теоретических основах химической технологии, технологических процессах и типовых аппаратах основных химических производств, проблемах и перспективах развития химической промышленности.
Наряду с использованием технологии основных химических производств в нем рассматриваются и практические результаты использования химических законов, экспериментальных методов, а также химических продуктов в различных отраслях экономики и в социально-бытовой сфере. Современное состояние общества характеризуется проникновением химии во все сферы жизни. Самые разнообразные химические вещества используются сегодня в промышленности и сельском хозяйстве, в строительстве и энергетике, в медицине и в быту. Необходимо ориентироваться в том, как получаются те или иные химические вещества, какие природные маете риалы используются для этого. Немаловажными представляются и экологические проблемы современной химической технологии, проблеме комплексного использования природного сырья, энергетические [4, 44, 45].
Изучение принципов химической технологии невозможно без количественных расчетов. Студент, избравший химическую специальность, должен овладеть в совершенстве простейшими приемами умственной деятельности, развивать творческое мышление. Важным компонентом этого процесса является умение решать химические задачи, так как оно всегда связано с более сложной мыслительной деятельностью [20].
1.2 Трактовка понятия «задача»
Психологи и дидакты по-разному трактуют понятие «задача», связываю его с другими родственными понятиями. По словам А.И. Леонтьева, «задача – это цель, данная в определенных условиях». При характеристике процессов мышления задачу определяют как ситуацию, в которой субъект для достижения сформулированной цели должен выяснить неизвестное на основе использования его связи с известным. Л.М. Фридман считает, что задача – это «знаковая модель проблемной ситуации». По определению Я.А. Пономарева, «задача есть ситуация, которая определяет действие субъекта, удовлетворяющего потребность путем изменения ситуации». В кибернетике для определения задачи вместо понятия «субъект» вводится понятие «решающая система», это расширяет возможности средств решения задачи: задачу может решать машина. Человек в отличие от машины не только решает строго поставленные задачи, но и совершенствует процесс познания, добиваясь новых теоретических и практических результатов. Решение задачи есть вид творческой деятельности, а поиск решения – процесс изобретательства. Учебную же задачу принято считать частным случаем задачи вообще. Таким образом, основным содержанием задач являются проблемные ситуации, решение которых возможно в результате творческого поиска. При этом необходимо учитывать как специфику предмета, так и психологические закономерности процесса решения.
Химическая учебная расчетная задача – это модель проблемной ситуации, решение которой требует от учащихся мыслительных и практических действий на основе знания законов, теорий и методов химии, направленная на закрепление, расширение знаний и развитие химического мышления.
Решение задач не самоцель, а цель и средство обучения и воспитания. В связи с этим проблема решения задач является одной из основных для дидактики, педагогической психологии и частных методик [57].
1.3 Значение химической задачи в процессе обучения
Решение задач занимает в химии важное место. Во-первых, это один из приемов обучения, посредством которого обеспечивается более глубокое и полное усвоение ученого материала по химии и вырабатывается умение самостоятельного применения приобретенных знаний на практике. Во-вторых, это прекрасный способ осуществления межпредметные и курсовых связей и связи химической науки с жизнью. Успешное решение задач учащимися, поэтому является одним из завершающих этапов в самом познании. Чтобы научиться химии, систематическое изучение известных истин химической науки должно сочетаться с самостоятельным поиском решения сначала малых, а затем и больших проблем.
Решение задач требует умения логически рассуждать, планировать, делать краткие записи, производить расчеты и обосновать их теоретическими предпосылками, дифференцировать определенные проблемы в целом. При этом не только закрепляются и развиваются знания и навыки учащихся, полученные ранее, но и формируются новые. Задачи, включающие определенные химические ситуации, становятся стимулом самостоятельной работы учащихся над учебным материалом, являются средством контроля и самоконтроля, помогает определить степень усвоения знаний и умений и их использования на практике; позволяет выявлять пробелы в знаниях и умениях учащихся и разработать тактику их устранения. При решении задач развивается кругозор, память, речь, мышление учащихся, а также формируется мировоззрение в целом; происходит сознательное усвоение и лучшее понимание химических теорий, законов и явлений. Решение задач развивает интерес учащихся к химии, активизирует их деятельность, способствует трудовому воспитанию школьников и их политехнической подготовке [1, 55, 57].
Отсюда понятно общепринятое в методике мнение, что мерой усвоения материала следует считать не только и даже не, сколько пересказ учебника, сколько умение использовать полученные знания при решении различных задач.
Психологи и дидакты рассматривают решение задач как модель комплекса умственных действий. Мышление при этом выступает как проблема «складывания» операций и определенную систему знаний с ее последующим обобщением. Значительна роль задач в организации поисковых ситуаций необходимых при проблемном обучении, а также в осуществлении процесса проверки знаний учащихся и при закреплении полученного материла [20].
Психологический анализ обучения свидетельствует о том, что усвоение знаний происходит в процессе активной мыслительной работы учащегося при решении им задачи через выделение существующих сторон проблемы путем анализа, абстрагирования и обобщения. Правильно подобранные задачи в соответствии с уровнем развития учащихся не только реализуют их психологически потенциал, но и мобилизует личность в целом, охватывая эмоциональную сферу, интересы, потребности. По наблюдениям психологов, учителей и методистов сверхтрудные задачи, превышающие известный барьер сложности, не только не стимулируют, а наоборот, снижают уровень мышления и не приносят пользы. Чтобы задачи будили мысль и развивали мышление, они должны быть посильны. Тогда мысль учащегося последовательно переходит от одного объекта к другому, это приковывает его внимание к задаче и стимулирует дальнейшее решение.
Итак, решение задач с психолого-педагогической точки зрения:
- учить мыслить учить мыслить, ориентироваться в проблемной ситуации;
- предполагает активную продуктивную деятельность с определенной глубиной, широтой и самостоятельностью решения, которая должна быть направлена на установление переноса знаний на новые объекты;
- проявляет взаимосвязь представлений и понятий;
- ведет к лучшему пониманию учащимися явлений в свете важнейших теорий;
- позволяет устанавливать связи химии и другими предметами, особенно с физикой и математикой;
- является средством закрепления в памяти учащихся химических законов и важнейших понятий;
- служит одним из способов учета знаний и проверки навыков, полученных в процессе изучения предмета;
- воспитывает в процессе изучения учащихся умение использовать полученные знания для решения практических проблем, тем самым, связывая обучение с жизнью и деятельностью человека [57].
Итак, исходя из выше указанной роли задач в курсе изучения химии, при решении задач ставятся следующие цели:
Образовательная цель.
- усвоение, закрепление, систематизация и совершенствовании учебного материала, формирование важных структурных элементов знаний, осмысление химической сущности явлений;
- выработка умения применять приобретенные знания самостоятельно в конкретно заданной ситуации, т.к. формирование теорий и законов, запоминание правил, формул, составление химических уравнений происходит в действии;
Процесс решения задачи – это познавательный процесс, это восхождение от абстрактного к конкретному. В методологическом аспекте – это подход от абстрактного мышления к практике, связь частного с общим.
Необходимо помнить, что решение задач – это не самоцель, а средство обучения, способствующее прочному усвоению знаний.
Воспитательная цель.
- формирование мировоззрения, осознанием материала, расширение кругозора в краеведческих и политехнических вопросах;
- реализация межпредметных связей, показывающие единство природы, связи обучения с жизнью, что позволяет развивать мировоззрение учащихся.
- осуществление принципа политехнизма;
- воспитание трудолюбия, целеустремленности, развитие чувства ответственности, упорства и настойчивости в достижении поставленной цели;
Развивающая цель.
- в ходе решения задач идет сложная мыслительная деятельность учащихся, которая определяет развитие, как содержательной стороны мышления (знаний), так и действенной (операций, действия).
- формирование научно-теоретического, логического, творческого мышления, развитие смекалки, в будущем – изобретательности и ориентацию на профессию химика.
- теснейшее взаимодействие знаний и действий является основой формирования различных приемов мышления: суждений, умозаключений, доказательств.
Решение задач – это мыслительный процесс.
Знания, используемые при решении задач, можно подразделить на два рода: знания, которые учащиеся приобретают при разборе текста задачи и знания, без привлечения которых процесс решения невозможен. Сюда входят различные определения, знания основных теорий и законов, разнообразные химические понятия, физические и химические свойства веществ, формулы соединений, уравнения химических реакций, молярные массы веществ и т.п [1, 27, 52, 51, 57].
1.4 Требования к изучению химической задачи и ее место в процессе обучения
Методика обучения определяется как педагогическая наука, исследующая закономерности определенному учебному предмету. Соответственно, методика обучения учащихся решению задач по химии может представлять частную методику, исследующую закономерности обучения решению задач.
Овладение методикой обучения школьников решать задачи — одно из сложных профессиональных умений учителя химии. В приобретении этого умения студентам помогут специально организованные практические занятия на семинаре. Занятиям предшествует работа студентов по небольшому методическому руководству — они выполняют определенные заданий и знакомятся с вопросами, которые будут подниматься на семинаре [38, 39].
Решение химических задач – важная сторона овладения знаниями основ науки химии. Включение задач в учебный процесс позволяет реализовать следующие дидактические принципы обучения:
1) обеспечение самостоятельности и активности учащихся;
2) достижение прочности знаний и умений;
3) осуществление связи обучения с жизнью;
4) реализация политехнического обучения химии, профессиональной ориентации.
В решении задач должен соблюдаться единый методический подход. Ведущая роль в обучении учащихся решению задач принадлежит учителю. Но нельзя недооценивать самостоятельности и учащихся при решении задач. При переходе от одного этапа к другому следует руководствоваться рекомендациями по формированию умений. Рассмотрим сущность этих этапов [52].
Выбирая задачу для учащихся, учитель обязан оценить ее с точки зрения следующих целей.
1. Какие понятия, законы, теории, факты должны быть закреплены в процессе решения, какие стороны свойств изучаемого вещества и химические реакции отмечены в процессе решения.
2. Какие приемы решения задачи должны быть сформированы.
3. Какие мыслительные приемы развиваются в процессе решения задачи.
4. Какие дидактические функции выполняют данные задачи.
Психологические исследования проблемы обучения решению задач показывают, что несформированность умений является следствием причин, которые обучающиеся просто не принимают во внимание. Природа внимания у учащихся такова, что они не способны долго концентрировать его на данном предмете. Зачастую длительное решение однотипных задач приводит к тому, что учащиеся решают новую предложенную задачу по тому старому образцу, который предложен преподавателем и не пытаются сделать это нестандартными способами, по-своему, не замечая, что ситуация в целом изменилась. Решая задачу, не осознают должным образом свою собственную деятельность, т.е. не понимают сущности задач и хода их решения. Не всегда анализируют содержание задачи, проводят ее осмысление и обоснование. Не вырабатывают общие подходы к решению, не определяют последовательности действий. Часто неправильно используют химический язык, математические действия и обозначения физических величин. На первое место при решении задач ставятся получение ответа любым действием, а не объяснение хода решения. При решении химической задачи не выделяют ее химическую часть и математические действия. Не задают цель проверить правильность результата не по ответу в задачнике, а решение обратной задачи или другим способом. Не вырабатывают понимания определенной системы задач, и они представляются бесформенным скоплением различных типов, видов, не связанных друг с другом. Для тех, кто сможет преодолеть эти недостатки, решение задач не будет вызывать особых трудностей. Процесс решения станет увлекательным, и будет приносить удовлетворение, подобно тому, которое получают любители разгадывания кроссвордов.
Умение решать задачи развивается в процессе обучения, и развивать это умение можно только одним путем – постоянно систематически решать задачи!
Поэтому, если ставится цель – закрепление теоретического материала, то метод решения задач должен быть уже известен учащимся. Если объясняется новый тип задач по методу решения, то учащиеся должны свободно оперировать учебным материалом. Одновременно обе цели ставить не рекомендуется [38].
Учитель активизирует знания учащихся, которые используются при решении задач. Затем приводится анализ условия задачи. Учитель кратко его записывает с помощью символов и условных обозначений. Далее разрабатывают план решения и по возможности выражают его в общем виде с помощью указанных выше формул, соблюдая все правила, которым учащиеся на уроках математики и физики. Тонко после этого приступают к числовому решению и проверяют ответ.
Если цель решения – изучение нового типа задач, то четко формулируют алгоритм, который учащиеся записывают и отмечают, к какому типу решения он соответствует. После чего решается аналогичная задача и предлагается задачи для самостоятельного решения.
Исходя их выше сказанного, вытекает место задач в процессе обучения.
При объяснении нового материала задачи помогают иллюстрировать изучаемую тему конкретным практическим применением, в результате учащиеся более осознанно воспринимают теоретические основы химии.
Использование задач при закреплении новой темы позволяет учителю выявить, как усвоен новый материал, и наметить методику и план дальнейшего изучения данного вопроса.
Решение задач дома способствует привлечению учащихся к самостоятельной работе с использованием не только учебников, но и дополнительной справочной литературы.
С целью текущего, а также итогового контроля и учета знаний лучшим методом является также расчетная задача, т.к. при ее решении можно оценить все качества ученика, начиная от уровня знания теории до умения оформлять решение в тетради.
Особое место занимает решение задач при повторении и обобщении учебного материала. Именно здесь в большей степени реализуются межпредметные связи, а также системность и целостность изучаемой темы или курса в целом [57].
1.5 Система химических задач
При всей важности отдельных задач эффект целостного образовательного процесса обеспечивается всем множеством задач по каждой теме, которое должно образовывать систему. Таким образом, ключевой элемент ресурсного обеспечения учебного процесса — система задач.
Системой задач называется совокупность задач к блоку изучаемой теме, удовлетворяющая ряду требований.
1. Полнота. В системе задач присутствуют задачи на все изучаемые понятия, факты, способы деятельности, включая мотивационные, подводящие под понятие, на аналогию, следствия из фактов и пр.
2. Наличие ключевых задач. Задачи сгруппированы в узлы вокруг объединяющих центров - задач, в которых рассматриваются факты или способы деятельности, применяемые при решении других задач и имеющие принципиальное значение для усвоения предметного содержания.
3. Связность. Вся совокупность задач может быть представлена связным графом, в узлах которого - ключевые задачи, выше них — подготовительные и вспомогательные, ниже — следствия, обобщения и т. д.
4. Возрастание трудности в каждом уровне. Система состоит из трех подсистем, соответствующих минимальному, общему и продвинутому уровням планируемых результатов обучения. В каждой из подсистем трудность задач непрерывно нарастает.
5. Целевая ориентация. Для каждой задачи определено ее место и назначение в блоке изучения материала.
6. Целевая достаточность. В системе достаточно задач для тренажа, аналогичных задач для закрепления методов решения, задач для индивидуальных и групповых заданий разной направленности, для самостоятельной (в том числе исследовательской) деятельности учащихся, для текущего и итогового контроля с учетом запасных вариантов и т. д.
7. Психологическая комфортность. Система задач учитывает наличие разных темпераментов, типов мышления, видов памяти.
Система задач - основной ресурс учителя для реализации эффективного образовательного процесса. От качества этого ресурса более чем наполовину зависит успех учащихся при изучении курса. Остальные составляющие успеха заключены в организации их деятельности и управлении этой деятельностью [19, 39].
1.6 Этапы решения задач
Психологами обнаружена закономерность в поведении человека при решении задач. Он разбивает задачу на некоторые число более простых, т.е. ставит пред собой промежуточные вопросы (анализ задачи). Затем приступает к очередной проверке ряда простых задач, накапливая количественную информацию. Решив их, переходит к решению сложной – синтезирует. Таким образом, задачи решаются путем анализа и синтеза в совокупности. Иногда анализ протекает в скрытом виде (решающий провел анализ быстро, по шаблону), в таком случае создается впечатление, что имеет место только синтез. Поэтому цель учителя – не только подобрать задачи к уроку, но и обдумать, как он будет обучать учащихся разбивать подобранные задачи на более простые.
Решение задачи состоит из многих операций, которые связаны между собой и применяются в некоторой логической последовательности. Выявление этих связей и определение последовательности логических и математических операций лежат в основе умения решать задачи.
Решение предполагает поисковую деятельность, включение в этот процесс интеллектуальных операций. С точки зрения дидактики важно иметь в виду и то обстоятельство, что при решении любой задачи (математической, физической, химической и др.) задаются цель, условия и требования к учебно-познавательной деятельности. Естественно предположить существование закономерностей для процесса овладения общей процедурой деятельности. Отсюда вытекает необходимость использования общей методологии решения задач, т.е. объективном процессе интеграции естественнонаучных и математических знаний и умений, неизбежности связи предметных языков. Таким образом, главная дидактическая цель учителя химии при обучении решению расчетных задач: формирование общих логических основ стехиометрических знаний и общепредметных умений на базе общенаучных методов.
В общем виде способ решения химических задач можно представить следующим порядком действий:
1) краткая запись условия задачи (вначале указывают буквенные обозначения заданных величин и их значения, а затем — искомые величины), которые при необходимости приводятся в единую систему единиц (количественны сторона);
2) выявление химической сущности задачи, составление уравнений всех химических процессов и явлений, о которых идет речь в условии задачи (качественная сторона);
3) соотношения между качественными и количественными данными задачи, т.е. установление связей между приводимыми в задаче величинами с помощью алгебраических уравнений (формул) – законов химии и физики;
4) математические расчеты [15, 57].
1.7 Классификация химических задач
В ходе составления условий простейших задач и их решения необходимо научиться классифицировать задачи, понимать взаимосвязь между различными величинами, характеризующими условие задачи, т. е., прежде чем приступить к решению задачи, необходимо проанализировать ее условие.
На сегодняшний день не существует окончательной едино разработанной классификации химических задач. В учебных пособиях по методике химии, специальных методических пособиях по решению задач и в статьях приводятся различные классификации задач. Общепризнанной является классификация задач на количественные и качественные, которые решаются устным письменным и экспериментальным способом. В свою очередь эти задачи бывают репродуктивными и продуктивными. Репродуктивные задачи – это типовые задачи, при решении которых возможно применение алгоритмов. В этом случае учитель сам объясняет ход их решения. Продуктивные – творческие задачи, в них необходимо самостоятельно найти способы решения. Для этого не достаточно организованного опыта, необходимо качественно иной опыт, заключающийся в умении логически мыслить, анализировать ситуацию в способности к интуитивному решению проблемы как высшего проявления логического мышления [20, 57].
Различаются задачи и упражнения по дидактическим целям. Задачи имеют целью развитие у учащихся умения применять знания химии в различных условиях практики. Упражнения имеют в качестве основных целей формирование навыков, но отдельным операциям, умственным или физическим. Следовательно, знание различия понятий «упражнения» и «задачи» имеет не только теоретическое, но и практическое значение, так как позволяет целесообразно применять упражнения или задачи обучении.
2. Выявление трудностей при решении задач по теоретическим основам химической технологии в рамках изучения курса Прикладная химия
Задачи по химической технологии, составленные и подобранные в настоящей работе, были использованы для проведения контрольной работы по прикладной химии. В апробации участвовали студенты 5 курса специальностей «Химия» с доп. спец. «Биология» и «Биология» с доп. спец. «Химия» (всего 39 студентов). Контрольная работа проводилась на итоговом занятии по прикладной химии. Каждая задача оценивалась по 5-балльной системе в соответствии с тем, насколько полно представлено решение. Оценка за контрольную работу в целом также выставлялась по 5-балльной системе, принятой в ВУЗах.
Практически все студенты справились с задачами (92,3%), в том числе 61,8% на «хорошо» и «отлично» (рис. 1). И действительно, большинство студентов не испытывали трудностей в решении задач. Наиболее успешно были решены задачи по химической технологии с производственным содержанием (металлургия – полностью решили 66,7% студентов, производство органических соединений – 61,5%, рис. 2). Некоторые затруднения вызвало решение задач на темы химическая кинетика и химическое равновесие (полностью эти задачи решили около 40% студентов), возможно, из-за сложного математического аппарата этих задач, где требуется знание основ интегрирования, дифференцирования, возведения в степень и т.д.
Мы проанализировали решение каждого типа задач. Многие студенты не получили высокие баллы за контрольную работу из-за того, что не получили правильные итоговые ответы. Действительно, достаточно большая часть ребят решила задачи «не полностью» (рис. 3, 4). Как правило, такие студенты приводили верные формулы для расчетов, но затруднялись в подстановке численных значений.
Конкретные, наиболее часто встречающиеся ошибки в решении задач представлены в табл. 1.
Таблица 1.
| Тема |
Результаты контрольной работы, % |
Замечания |
||
| Решили полностью |
Не решили |
Решили не полностью или с ошибками |
||
|
Термохимия |
46,2% | 12,8% | 41% | Ошибки связаны в основном с уравнениями химических реакций, студенты забывают расставить коэффициенты, а также ошибки связанные со следствиями из закона Гесса. |
|
Химическое равновесие |
41% | 15,4% | 43,6% | Ошибки связаны с нахождением константы равновесия: студенты «переворачивают» формулу для нахождения Кс, а также коэффициенты перед веществами ставят как множители, а не как степень. Не помнят о знаке «-» в уравнении Вант-Гоффа (зависимость константы равновесия от температуры). Также наблюдаются затруднения при нахождении равновесных концентраций, если известна константа равновесия (с использование перемен. х) |
|
Химическая кинетика |
38,5% | 20,5% | 41% | Ошибки связаны с определением порядка реакций. Многие студенты забывали о присутствии экспоненты и предэкспоненциального множителя в уравнении Аррениуса. |
|
Технико-экономические показатели производств |
59% | 10,3% | 30,7% | Ошибки связаны с неправильным нахождением выхода продукта и с незнанием формул для расчета степени превращения исходных реагентов и селективности. |
|
Задачи с экологическим содержанием |
51,3% | 8% | 30,7% |
Ошибки связаны с
непони-манием сущности задачи, а также ошибки связанные с неправильным
переводом м3 в литры, и с неправиль-ным использованием значения
массы вещества вместо объема раствора в формуле |
|
Металлургия |
66,7% | 7,7% | 25,6% |
Ошибки связаны с непра-
вильным нахождением mпр и mтеор. В формуле |
|
Электрохимические производства |
56,7% | 12,8% | 30,2% | Ошибки связаны с непра- вильным нахождением эквивалента элемента, с неправильным переводом часов в секунды (система СИ). |
|
Производство органических соединений |
61,5% | 7,7% | 30,8% |
Ошибки связаны с непра- вильным нахождением молекулярной массы вещества, с неправильным определением брутто – формулы вещества |
Общие ошибки:
1. неправильное нахождение молекулярной массы вещества.
2. не знание правил округления числовых значение, что в итоге приводит
к неправильному нахождению ответа.
3. Ошибки, связанные с подсчетом ех, ln x, 10x и т.д. на калькуляторе.
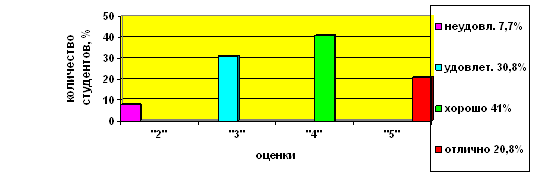
Рис. 1. Оценки, полученные студентами на контрольной работе по прикладной химии
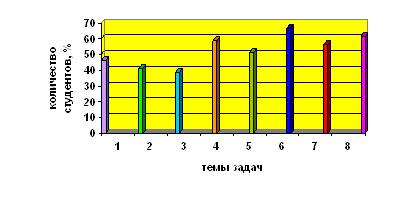
1- Рис. 2. Доля студентов, полностью решившая задачи по отдельным темам. термохимия, 46.2%
2- химическое равновесие, 41%
3- химическая кинетика, 38.5%
4- технико-экономические показатели, 59%
5- задачи с экологическим содержанием, 51.3%
6- металлургия, 66.7%
7- электрохимические производства, 56.4%
8- производство органических соединений, 61.5%
Таким образом, апробация задач по химической технологии среди студентов 5 курса на итоговой контрольной работе показала необходимость повторения в курсе основы химической технологии базовых тем по физической химии (химическая кинетика, термодинамика, электрохимия и т.д.) и высшей математике (дифференцирование, интегрирование, степенные функции и т.д.). Реальной помощью для самостоятельной проработки этого фактически уже хорошо известного студентам материала может послужить пособие по прикладной химии «Задачи по теоретическим основам химической технологии», составленное по материалам представленной работы.
3. Методика решения задач по теоретическим основам химической технологии
Одна из главных задач химической науки и промышленности - получение необходимых человеку веществ (продуктов, материалов). Поэтому большинство учебных химических задач снизано с расчетами по уравнению химической реакции, которую в общем виде можно представить так:
аА+ вВ ![]() cC+dD
cC+dD
где A, В, С, D - условные обозначения формул различных веществ;
а, в, с, d — стехиометрические коэффициенты.
Расчет по уравнению реакции наиболее прост лишь в идеальном случае, когда реагенты абсолютно чистые, взяты в строго стехиометрических отношениях, потерь при реакции нет, т.е. выход продукта составляет 100%. Практически эти условия не выполняются. Как правило, исходные вещества содержат примеси или взяты в виде растворов; обычно одно из веществ, вступающих в реакцию (наиболее доступное, дешевое, берут в избытке и, наконец, реальный выход продуктов всегда меньше 100%.)
Итак, химические задачи делят на:
1) Расчетные
2) Качественные
Расчетные задачи условно делятся на две группы:
1) Задачи, решаемые с использованием химической формулы вещества или на вывод формулы.
2) Задачи, для решения которых используют уравнения химических реакций.
3) Задачи, для решения которых используют только математические формулы.
Первая группа задач включает расчеты по определению массы чистого вещества в смеси (растворе) по известной массовой доле его (или процентному содержанию); вычисление массовой доли (или процента) элементов по формулам веществ (прямая и обратная задачи).
Ко второй группе задач относятся вычисления по химическим уравнениям массы, объема и количества продуктов реакции или взаимодействующих веществ в различных единицах измерения. При этом учитывают произвольное соотношение компонентов, т. е. наличие избытка одного из реагирующих веществ; практический выход продукта реакции; наличие примесей в исходных веществах или продуктах реакции.
На уроках обобщения знаний о химических производствах составляются задачи с производственным содержанием. Совместно с учащимися определяем, какие особенности таких задач следует при этом учитывать:
1) условия процесса (концентрация, давление, температура);
2) возможность протекания процесса;
3) кинетику и равновесие реакций;
4) состав сырья (наличие примесей, необходимость очистки);
5) выход продукта (потери в процессе очистки; обратимость процесса; побочные реакции; циркуляция);
6) использование энергии экзотермических процессов;
7) утилизация побочных продуктов и отходов производства.
8) экологический аспект;
9) технико-экономические показатели химических производств;
10) использование электрической энергии. [54]
При составлении методического пособия для решения задач по химической технологии мы условно выделили несколько разделов задач по их химической тематике:
I. Общие вопросы химической технологии.
1. термохимия.
2. химическая кинетика.
3. химическое равновесие.
II. Технико-экономические показатели химических производств.
III. Задачи с экологическим содержанием.
IV. Производство неорганических соединений.
1. металлургия.
2. электрохимические производства.
V. Производство органических соединений.
VI.Творческие и изобретательские задачи.
Каждый раздел задач сопровождается методической частью, где приводятся основные теоретические аспекты темы, законы и формулы для математических расчетов. Далее рассматриваются методические рекомендации по решению задач, конкретные примеры решения типичных и наиболее сложных задач, а также задачи для самостоятельного решения. Эти задачи могут быть использованы на практических занятиях, для проведения коллоквиумов, индивидуального собеседования при защите лабораторных работ, а также в средней общеобразовательной школе при изучении факультативного курса по химии.
3.1 Общие вопросы химической технологии
3.1.1 Термохимия
Термохимия — учение о тепловых эффектах химических реакций. Для решения задач по термохимии необходимо знать такие понятия, как тепловой эффект реакции, стандартная тепловой эффект образования вещества, стандартная тепловой эффект сгорания химического соединения, закон Гесса и следствия из него, возможность самопроизвольного протекания реакции, зависимость энергии Гиббса от температуры. Наиболее важным понятием химической энергетики является тепловой эффект химической реакции. Данные о тепловых эффектах применяются для определения строения и реакционной способности соединений, энергии межатомных и межмолекулярных связей, используются в технологических и технических расчетах. В основе термохимических расчетов по уравнениям реакций лежит закон сохранения и превращения энергии, или первое начало термодинамики. Сущность его состоит в том, что при всех превращениях энергия не возникает и не исчезает, а одни ее виды переходят в эквивалентные количества других видов. Количество выделившейся (поглощенной) теплоты в результате химической реакции называется тепловым эффектом реакции Q (при p-const QP или V-const QV) (измеряется в кДж). По тепловому эффекту химические реакции подразделяются на экзотермические (с выделением теплоты (+Q)) и эндотермические (с поглощением теплоты (-Q)). Существует величина обратная тепловому эффекту (записывается с противоположным знаком). Она характеризует внутреннюю энергию вещества и называется энтальпией (∆Н). Изменение энтальпии измеряют в кДж/моль, т.е. это то количество теплоты, которое выделяется или поглощается при образовании 1 моль вещества из простых веществ. С термодинамической точки зрения принимают, что тепловой эффект при постоянном давлении и температуре равен изменению энтальпии ΔН. Передачу энергии при этом рассматривают как бы со стороны самой реакционной системы. Если система отдала энергию во внешнюю среду, величина ΔН считается отрицательной ΔН<0, если реакционная система получила энергию за счет внешней среды — величину ΔН считают положительной ΔН>0. Вычисление теплоты реакции по теплотам образования участвующих в ней веществ, производится на основании закона Гесса.
Закон Гесса: Тепловой эффект химической реакции при постоянном давлении и объеме не зависит от пути реакции (т.е. от промежуточных стадий), а определяется начальным и конечным состоянием системы (т.е. состоянием исходных веществ и продуктов реакции (газ, жид., тв.)).
ΔrН0298 – стандартная энтальпия реакции (reaction), тепловой эффект реакции.
ΔfН0298 – стандартная энтальпия образования (formation) 1 моль вещества из простых веществ в стандартных условиях (Т=298К или 25С, Р=1 атм.), на которые указывает знак «0», (кДж/моль).
ΔсН0298 – стандартная энтальпия сгорания (combustion) 1 моль вещества (до образования СО2, Н2О, и др. продуктов), (кДж/моль).
Следствие 1 из закона Гесса:
Тепловой эффект химической реакции равен разности между алгебраической суммой теплот образования продуктов реакции и алгебраической суммой теплот образования исходных веществ
ΔrН0298 =∑(nj •ΔfН0298)прод - ∑(ni• ΔfН0298)исх.
где, nj и ni – количество вещества продуктов реакции и исходных веществ соответственно (численно равно коэффициенту в уравнении реакции), (моль).
Следствие 2 из закона Гесса:
Тепловой эффект химической реакции равен сумме теплот сгорания исходных веществ минус сумма теплот сгорания продуктов реакции
ΔrН0298 =∑(ni• ΔсН0298) - ∑(nj• ΔсН0298)
где, ni и nj - количество вещества исходных веществ и продуктов реакции соответственно (численно равно коэффициенту в уравнении реакции), (моль).
В химических реакциях может одновременно изменяется и энергия системы и ее энтропия, поэтому реакция протекает в том направлении, в котором общая суммарная движущая сила реакции уменьшается. Если реакция происходит при постоянном температуре и давлении, то общая движущая сила реакции называется энергией Гиббса (ΔG0) и направление реакции определяется ее изменением.
Зависимость энергии Гиббса реакции от температуры описывается уравнением
ΔG0T=ΔH0T – TΔS0T
При стандартной температуре
ΔG0298=ΔH 0298– TΔS0298
ΔG0298 – стандартная энергия Гиббса, изменение энергии Гиббса при образовании 1 моль вещества из простых веществ в стандартных условиях, (кДж/моль).
Стандартную энергию Гиббса реакции рассчитывают по первому следствию из закона Гесса.
∆rG 0298= ∑(njΔfG0298) прод. -∑ (niΔfG0298)исход.
ΔS0298 - стандартная энтропия 1 моль вещества в стандартном условиях, (Дж/К*моль). Энтропию можно характеризовать как меру беспорядка (неупорядоченности) системы. Эта величина характеризует изменение температуры в системе.
Поскольку энтропия – функция состояния системы, ее изменение (ΔS) в процессе химической реакции можно подсчитать, используя следствие из закона Гесса.
ΔrS0298 =∑ (njΔfS0298) прод. –∑(niΔfS0298)исход
где, nj и ni – количество вещества продуктов реакции и исходных веществ соответственно (численно равно коэффициенту в уравнении реакции), (моль).
ΔrS0298 =∑ (niΔfS0298) исход –∑(njΔfS0298)прод
где, ni и nj - количество вещества исходных веществ и продуктов реакции соответственно (численно равно коэффициенту в уравнении реакции), (моль).
ΔrS0298 – стандартная энтропия реакции, (Дж/К).
ΔfS0298 – стандартная энтропия образования химического вещества, (Дж/К*моль).
Знак « - » перед членом TΔS0298 (энтропийным членом) ставится, для того чтобы при ΔH=0 сделать ∆G отрицательной величиной ΔG<0 – условие самопроизвольного протекания реакции.
Если пренебречь изменением ΔS0 и ΔН0 с увеличением температуры, то можно определить Травн, т.е. температуру, при которой устанавливается химическое равновесие химической реакции для стандартного состояния реагентов, т.е. из условия равновесия реакции ΔG=0 имеем 0=ΔrH 0298– TΔrS 0298, отсюда
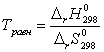
![]()
Следует знать:
Если ΔS=0 (ΔS>0), ΔH<0(ΔH=0) то ΔG <0 – реакция протекает самопроизвольно, процесс протекает в прямом направлении (энергетически выгоден).
Если ΔS=0(ΔS<0), ΔH>0 (ΔH=0) то ΔG>0 – протекание реакции невозможна, возможна только в обратном направлении (энергетически невыгоден).
Если ΔS=0, ΔH=0 ΔG=0 – система находится в состоянии равновесия.
Примеры решения задач
1. Вычислить тепловой эффект реакции получения гидроксида кальция
СаО(т) + Н2О(ж) = Са(ОН)2(т), если теплота образование СаО(т) равна +635701,5Дж/моль, теплота образования Н2О(ж) +285835,5 Дж/моль и теплота образования Са(ОН)2 +986823 Дж/моль.
Решение:
Тепловой эффект реакции
СаО (т) + Н2О (ж) = Са(ОН)2(т) по первому следствию закона Гесса, будет равен теплоте образования Са(ОН)2(т) минус теплота образования Н2О(ж) и теплота образования (СаО(т)):
ΔrН0298 =∑(nj •ΔfН0298)прод - ∑(ni• ΔfН0298)исх.
ΔrН0298=1 моль•ΔfН0298(Са(ОН)2(т)) - (1 моль ΔfН0298(СаО(т)) +
+1 моль• ΔfН0298(Н2О (ж)))=1 моль*986823 Дж/моль - (1 моль* 635701,5 Дж/моль +
+ 1 моль*285835,5 Дж/моль)= 65 286 Дж.
Ответ: 65286 Дж.
2. Вычислите изменения энергии Гиббса в реакции димеризации диоксида азота при стандартной температуре, при 0 и 100ºС. Сделать вывод о направлении процесса.
Решение:
При стандартной температуре 298 К изменение энтальпии в реакции
2NO2 (г) ![]() N2O4(г) равно
(первое следствие закона Гесса)
N2O4(г) равно
(первое следствие закона Гесса)
ΔrН0298 =∑(nj •ΔfН0298)прод - ∑(ni• ΔfН0298)исх.
Δ rН0298 =1 моль* 9660 Дж/моль – 2 моль*33800 Дж/ моль = - 57940 Дж
Изменение температуры равно
ΔrS0298 =∑ (nΔfS0298) прод. –∑(nΔfS0298)исход = 1 моль*304 Дж/моль*К -
–2 моль*234 Дж/моль*К = - 164 Дж/К
Зависимость энергии Гиббса реакции от температуры описывается уравнением
ΔG0T =ΔH0T – TΔS0T
При стандартной температуре
ΔrG0298=ΔH 0298– TΔS0298 = - 57940 Дж – (298 К*(-164 Дж/К)) = -9068 Дж/моль
Отрицательное значение энергии Гиббса реакции говорит о том, что смещении равновесия вправо (самопроизвольный процесс), т.е. в сторону образования диоксида азота.
При 0ºС (273К)
ΔrG0273 = -57940 Дж + 273К* 164 Дж/К = -13168 Дж/моль
Более высокое отрицательное значение ΔG273 по сравнению с ΔG0298 свидетельствует о том, что при 273 К равновесие еще больше смещено в сторону прямой реакции.
При 100ºС (373 К)
ΔrG373 = -57940 Дж + 373К*164 Дж/К = 3232 Дж/моль.
Положительная величина ΔG373 указывает на изменение направления реакции: равновесие смещено влево, т.е. в сторону распада димера N2O4 (реакция невозможна). Ответ: при 0ºС (273 К) ΔrG273= -13168 Дж/моль, реакция протекает самопроизвольно; при 100ºС (373 К) ΔrG373= 3232 Дж/моль, реакция невозможна.
3. Составьте термохимическое уравнение горения метана СН4 и рассчитайте объем воздуха, необходимый для сжигания 1моль метана, если известно, что при сгорании 5,6 л метана выделяется 220 кДж теплоты, содержание кислорода в воздухе равно 20%.
Решение:
СН4 + 2О2 = СО2 + 2Н2О, ∆Н<0
Находим количество вещества метана объемом 5,6 л
![]()
Если при сгорании СН4 количеством вещества 0,25 моль выделяется 220 кДж теплоты, то при сгорании СН4 количеством вещества 1 моль выделяется 880 кДж теплоты.
Термохимическое уравнение:
СН4 +2О2 = СО2+ 2Н2О+ 880 кДж
Из уравнения реакции видно, что на сгорание СН4 количеством вещества 1моль расходуется О2 количеством вещества 2 моль, на сгорание СН4 количеством вещества 0,25 моль расходуется х моль О2, откуда х = 0,5 моль.
Кислород количеством вещества 0,5 моль занимает объем 11,2 л.
В воздухе 20% кислорода, следовательно, объем воздуха будет равен
![]()
Ответ: 880 кДж, 56 л.
Задачи для самостоятельного решения
1. Рассчитайте, какая из ниже перечисленных реакций при стандартных условиях может идти самопроизвольно:
а) Fe(к) + Al2O3(к) = Al(к) + Fe2O3(к)
б) Al(к) + Fe2O3 (к)= Fe(к) + Al2O3(к)
в) CuSO4(к) + 2NH4OH(ж) = Cu(OH)2(к) + (NH4)2SO4(к)
г) Al2O3(корунд) + 3SO3 = Al2(SO4)2(к)
2. При сварке трамвайных рельсов используют термитную смесь, которую готовят, смешивая порошки алюминия и оксида железа (III) в количественном отношении 2:1. Термохимическое уравнение горения термитной смеси следующее: 2Al + Fe2O3= Al2O3 + 2Fe + 829,62 кДж. Сколько теплоты выделится при образовании: 1) 4 моль железа; 2) 1 моль железа?
3. Рассчитайте, достаточно ли теплоты, выделяющейся при сгорании 200 кг каменного угля, содержащего 82% углерода, для полного разложения 162 кг карбоната кальция, если для разложения 1 моль СаСО3 необходимо 180 кДж теплоты, а при сгорании 1 моль углерода, входящего в состав каменного угля, выделяется 402 кДж теплоты.
4. Процесс алюминотермии выражается химическим уравнением
8Al + 3 Fe3O4 = 4Al2O3 + 9Fe ΔH<0. Рассчитайте, сколько теплоты выделится при сгорании 1 кг термита.
5. Возможен ли обжиг колчедана массой 1т по следующему уравнению химической реакции 4FeS2 + 11O2 →2 Fe2O3 + 8SO2 ∆H<0
6. Вычислите тепловой эффект образования NH3 из простых веществ, при стандартном условии по тепловым эффектам реакции:
2H2 + O2 = 2H2O(ж) ΔН01 = -571, 68 кДж,
NH3 + 3O2 = 6H2O(ж) + 2N2 ΔН02 = -1530,28 кДж.
7. Стандартный тепловой эффект реакции сгорания этана равен -1560 кДж. Рассчитайте стандартную теплоту образования этана, если известно, что
ΔfН0298 (H2O)= -285,84 кДж/моль и ΔfН0298(СО2) = -396,3 кДж/моль.
8. Вычислите тепловой эффект реакции восстановления оксида железа водородом, пользуясь следующими данными.
FeO + CO = Fe + CO2 ΔН = -13,19 кДж
CO + 1/2O2 = CO2 ΔН = -283,2 кДж
2H2 + 1/2O2 = 2H2O(г) ΔН = -242 кДж
9. Протекание, какой из приведенных реакций восстановления оксида железа (III) наиболее вероятно при 298 К.
Fe2O3(k) + 3H2(г) = 2Fe(к) + 3H2O(к)
Fe2O3(k) + 3С(графит) = 2Fe(к) + 3СO(к)
Fe2O3(k) + 3СО(г) = 2Fe(к) + 3СО2(к)
10. В какой их перечисленных ниже реакций тепловой эффект ΔН0298 будет стандартной теплотой SO3(г)
а) S(г) + 3/2 O2 = SO3(г)
а) S(г) + 1/2 O2 = SO3(г)
а) S(к) + 3/2 O2 = SO3(г)
3.1.2 Химическое равновесие
При протекании химической реакции через некоторое время устанавливается равновесное состояние (химическое равновесие). Слово «равновесие» означает состояние, в котором сбалансированы все противоположно направленные на систему воздействия. Тело, находящееся в состоянии устойчивого равновесия, обнаруживает способность возвращаться в это состояние после какого-либо возмущающего воздействия.
Примером тела, находящегося в состоянии устойчивого равновесия, может служить шарик, лежащий на дне ямки. Если его толкнуть в одну или другую сторону, он вскоре снова возвращается в состояние устойчивого равновесия. В отличие от этого шарик, лежащий на краю ямки, находится в состоянии неустойчивого равновесия — достаточно ничтожного толчка, чтобы он необратимо скатился в ямку.
Оба этих примера являются примерами статического равновесия. В химии, однако, приходится сталкиваться не столько со статическими равновесиями, столько с динамическими («подвижными»). Динамическое равновесие устанавливается, когда оказываются сбалансированными два обратимых или противоположных процесса. Динамические равновесия подразделяют на физические и химические. Наиболее важными типами физических равновесий являются фазовые равновесия. Система находится в состоянии химического равновесия, если скорость прямой реакции равна скорости обратной реакции.
Например, если скорость протекания реакции (константа скорости к1)
k1
А(г) + В(пар) ![]() АВ(г)
АВ(г)
равна скорости обратной реакции (константа скорости k2)
k2
АВ(г)![]() А(г) + В(пар)
А(г) + В(пар)
то система находится в динамическом равновесии. Подобные реакции называются обратимыми, а их уравнения записывают с помощью двойной стрелки:
k1
А(г) + В(пар) ![]() АВ(г)
АВ(г)
k2
Реакции, протекающие слева направо, называются прямой, справа налево – обратной.
Нужно подчеркнуть, что реакционная система остается в состоянии динамического равновесия лишь до тех пор, пока система остается изолированной. Изолированной называют такую систему, которая не обменивается с окружающей средой ни веществом, ни энергией.
Состояние химического равновесия обратимых процессов количественно характеризуется константой равновесия. Так, для обратимой реакции общего вида
k1
аA +bB ![]() сC + dD (1.2.1)
сC + dD (1.2.1)
k2
константа равновесия К, представляющая собой отношение констант скорости прямой и обратной реакций, запишется
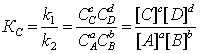 (1.2.2)
(1.2.2)
где, Кс – константа скорости реакции, зависящая от концентрации реагирующих компонентов; Сi или [ i ]- равновесная молярная концентрация i-того компонента;
a, b, c, d – стехиометрические коэффициенты веществ.
В правой части уравнения (1.2.2) стоят концентрации взаимодействующих частиц, которые устанавливают при равновесии, - равновесные концентрации.
Уравнение (1.2.2) представляет собой математическое выражение закона действующих масс при химическом равновесии. Для реакции с участием газов константа равновесия выражается через парциальные давления, а не через их равновесные концентрации. В этом случае константу равновесия обозначают символом Кр.
![]()
Рi - равновесные парциальные давления i-того компонента.
Сi - равновесная молярная концентрация компонентов.
a, b, c, d – стехиометрические коэффициенты веществ.
Состояние химического равновесия при неименных внешних условиях теоретически может сохраняться бесконечно долго. В реальной действительности, т.е. при изменении температуры, давления или концентрации реагентов, равновесии может «сместиться» в ту или иную сторону протекания процесса.
Изменения, происходящие в системе в результате внешних воздействий, определяется принципом подвижного равновесия – принципом Ле Шателье – Брауна. При воздействие на равновесную систему, любого внешнего фактора, равновесие в системе смещается в таком направлении, чтобы уменьшить воздействие этого фактора.
1. Влияние давления на равновесие химической реакции (для реакции, проходящей в газовой фазе).
aA + bB ![]() cC + dD
cC + dD
- если реакция идет с увеличением количества компонентов a + b < c + d, то повышение давления смещает равновесие химической реакции справа налево.
- если реакция идет с уменьшением количества компонентов a + b > c + d, при увеличении давления сдвиг равновесия произойдет слева направо.
- если количество компонентов одинаково a + b = c + d, то изменение давления не повлияет на положении равновесия.
2. Влияние инертного газа. Введение инертного газа подобно эффекту уменьшения давления (Ar, N2, водяной пар). Инертный газ не участвует в реакции.
3. Влияние изменения концентрации реагирующих веществ. При введение дополнительного количества вещества равновесие химической реакции сместиться в ту сторону где концентрация вещества уменьшается.
4. Влияние температуры на химическое равновесие реакции.
Если к равновесной системе подводится теплота, то в системе происходят изменения, чтобы ослабить это воздействие, т.е. процессы с поглощением теплоты. При экзотермических реакциях снижение температуру сместит равновесие слева направо, а при эндотермических реакциях повышение температуры сместит равновесие справа налево.
Зависимость Кр от температуры – уравнение Вант – Гоффа.
![]() ;
; ![]() ;
;
(![]() ); lnkT1 – lnkT2 =
); lnkT1 – lnkT2 = ![]()
Примеры решения задач
1. Реакция соединения азота и водорода обратима и протекает по уравнению
N2 + 3Н2 ![]() 2NН3.
При состоянии равновесия концентрации участвующих в ней веществ были: [N2]
= 0,01 моль/л, [Н2] = 2,0 моль/л, [NH3] = 0,40 моль/л.
Вычислить константу равновесия и исходные концентрации азота и водорода.
2NН3.
При состоянии равновесия концентрации участвующих в ней веществ были: [N2]
= 0,01 моль/л, [Н2] = 2,0 моль/л, [NH3] = 0,40 моль/л.
Вычислить константу равновесия и исходные концентрации азота и водорода.
Решение:
Для приведенной реакции
![]()
Подставляя значение равновесных концентраций, получим
![]() = 2
= 2
Согласно уравнению реакции из 1 моль азота и 3 моль водорода получаем
2 моль аммиака, следовательно, на образование 0,4 моль аммиака пошло
0,2 моль азота и 0,6 моль водорода. Таким образом, исходные концентрации будут [N2] = 0,01 моль/л + 0,2 моль/л = 0,21 (моль/л),
[H2] = 2,0 моль/л + 0,6 моль/л = 2,6 (моль/л).
Ответ: Кравн = 2; С0 (N2) = 0,21 моль/л и С0 (Н2) = 2,6 моль/л.
2. Один моль смеси пропена с водородом, имеющей плотность по водороду 15, нагрели в замкнутом сосуде с платиновым катализатором при 320°С, при этом давление в сосуде уменьшилось на 25%. Рассчитайте выход реакции в процентах от теоретического. На сколько процентов уменьшится давление в сосуде, если для проведения эксперимента в тех же условиях использовать 1 моль смеси тех же газов, имеющей плотность по водороду 16?
Решение:
С3Н6 + Н2 ![]() С3Н8
С3Н8
1) Пусть ν(C3H6) = х, ν(H2) =1-x, тогда масса смеси равна
42х + 2(1 - х) = 2 • 15 = 30,
откуда х = 0,7 моль, т. е. ν(C3H6) = 0,7 моль, ν(H2) = 0,3 моль.
Давление уменьшилось на 25% при неизменных температуре и объеме за счет уменьшения на 25% числа молей в результате реакции. Пусть у моль Н2 вступило в реакцию, тогда после реакции осталось:
ν(C3H6) = 0,7 - у, ν(H2) = 0,3 – у, ν(C3H8) = у,
νо6щ = 0.75 =(0,7 - у) + (0,3 - у) + у, откуда y = 0,25 моль.
Теоретически могло образоваться 0,3 моль С3Н8
(H2 — в недостатке), поэтому выход равен ![]() . Константа равновесия при
данных условиях равна
. Константа равновесия при
данных условиях равна
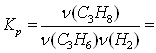
![]()
2) Пусть во втором случае ν(C3H6) = a моль, ν(H2) = (1 – а) моль, тогда масса смеси равна 42а + 2(1 - а) = 2 • 16 = 32, откуда, а= 0,75, т. е. ν(C3H6) = 0,75, ν(H2) = 0,25. Пусть в реакцию вступило b моль Н2. Это число можно найти из условия неизменности константы равновесия
![]() =
=![]()
Из двух корней данного квадратного уравнения выбираем корень, удовлетворяющий условию 0 < b < 0,25, т. е. b = 0,214 моль
Общее число молей после реакции равно
νoбщ =((0,75 - 0,214) + (0,25 - 0,214) + 0,214 - 0,786) моль, т. е. оно уменьшилось на 21,4% по сравнению с исходным количеством (1 моль). Давление пропорционально числу молей, поэтому оно также уменьшилось на 21,4%.
Ответ: выход С3Н8 — 83,3%; давление уменьшится на 21,4%.
Задачи для самостоятельного решения
1. В реакции между раскаленным железом и паром
3Fe(тв) + 4Н2О(г) ![]() Fe3O4(тв)+4Н2(г),
при достижении равновесия парциальные давления водорода и пара равны 3,2 и 2,4
кПа соответственно. Рассчитайте константу равновесия.
Fe3O4(тв)+4Н2(г),
при достижении равновесия парциальные давления водорода и пара равны 3,2 и 2,4
кПа соответственно. Рассчитайте константу равновесия.
2. Вычислите константы равновесия Кр КС газовой реакции
СО + Cl2 ![]() СОCl2, состав газовой смеси при
равновесии был следующим (% по объему): СО=2,4, Cl2 =12,6, СОCl2 =85,0, а общее давление
смеси при 20С составляло 1,033*105 Па. Вычислите ΔG реакции.
СОCl2, состав газовой смеси при
равновесии был следующим (% по объему): СО=2,4, Cl2 =12,6, СОCl2 =85,0, а общее давление
смеси при 20С составляло 1,033*105 Па. Вычислите ΔG реакции.
3. Рассчитайте константу равновесия при некоторой
заданной данной температуре для обратимой реакции СО + Н2О![]() СО2 + Н2,
учитывая, что в состоянии равновесия концентрации участвующих в реакции веществ
были равны [СО] = 0,16 моль/л, [Н2О] = 0,32 моль/л, [СО2]
= 0,32 моль/л, [Н2] = 0,32 моль/л.
СО2 + Н2,
учитывая, что в состоянии равновесия концентрации участвующих в реакции веществ
были равны [СО] = 0,16 моль/л, [Н2О] = 0,32 моль/л, [СО2]
= 0,32 моль/л, [Н2] = 0,32 моль/л.
4. В стальном резервуаре находятся карбонат кальция
и воздух под давлением 1 атм. при температуре 27°С. Резервуар нагревают до 800°С
и дожидаются установления равновесия. Вычислите константу равновесия Кр
реакции CaCO3![]() СаО + СО2 при 800°С,
если известно, что равновесное давление газа в резервуаре при этой температуре
равно 3,82 атм., а при 27°С СаСО3 не разлагается.
СаО + СО2 при 800°С,
если известно, что равновесное давление газа в резервуаре при этой температуре
равно 3,82 атм., а при 27°С СаСО3 не разлагается.
5. При постоянной температуре в гомогенной системе А + В = 2С установилось равновесие с равновесными концентрациями [А]=0,8 моль/ль, [В]=0,6 моль/л, [С]=1,2 моль/л. определите новые равновесные концентрации, если в систему дополнительно ввели 0,6 моль/л вещества В.
6. Как можно обосновать оптимальные условия промышленного синтеза аммиака с высоким выходом на основе термохимического уравнения реакции
N2 + ЗН2 ![]() 2NH3 + 491,8
кДж и с учетом того, что при низких температурах скорость прямой реакции очень
мала?
2NH3 + 491,8
кДж и с учетом того, что при низких температурах скорость прямой реакции очень
мала?
7. Вычислите константу равновесия ниже приведенных реакции, протекающей при стандартных условиях и при 400К.
а) Na2O(к) + CO2(г) → Na2CO3(к)
б) N2O4(г) = 2NO2(г)
8. Уравнение реакции окисления хлорида водорода
4НСl (г) + O2(г) = 2H2O(г) + 2Cl2(г) Вычислите константу равновесия этой реакции при Т=500К. Предположите способы увеличения концентрации хлора в равновесной смеси.
9. При смешении 2 моль уксусной кислоты и 2 моль этилового спирта в результате реакции СН3СООН + С2Н5ОН = СН3СООС2Н5 + Н2О к моменту наступления равновесия осталось 0,5 моль СН3СООН и С2Н5ОН, а также некоторое количество эфира и воды. Определите состав равновесной смеси, если смешивают по 3 моль СН3СООН и С2Н5ОН при той же температуре.
10. Вычислить начальные концентрации веществ в обратимой реакции
2СO +О2 ![]() 2СО2 и константу
равновесия, если равновесные концентрации составляют [СО]=0,44 моль/л, [О2]=0,12
моль/л, [СО2] =0,18 моль/л.
2СО2 и константу
равновесия, если равновесные концентрации составляют [СО]=0,44 моль/л, [О2]=0,12
моль/л, [СО2] =0,18 моль/л.
3.1.3 Химическая кинетика
Это раздел физической химии, изучающей скорость химических реакций, а в более широком смысле – закономерности их протекания.
Термин скорость реакции означает скорость, с которой образуются продукты, либо скорость, с которой расходуются агенты при протекании химической реакции. Химические реакции происходят с самыми разными скоростями. Со скоростью химических реакций связаны представления о превращении веществ, а также экономическая эффективность их получения в промышленных масштабах. Основным понятием в химической кинетике является понятие о скорости реакции, которая определяется изменением количества вещества реагентов (или продуктов реакции) в единицу времени в единице объема. Если при неизменном объеме и температуре концентрация одного из реагирующих веществ уменьшилась (или увеличилась) от значения с1 до значения с2 за промежуток времени от t1 до t2, то средняя скорость реакции составит
![]() (1.3.1)
(1.3.1)
где DСi – изменения концентрации i-того компонента, моль/м3 или моль/л,
wi - скорость реакции, (моль/(л • с) или моль/м3 *с). Уравнение (1.3.1) подходит для реакций протекающих в гомогенном реакционном пространстве.
Если реакция протекает в гетерогенном пространстве, то выражение для скорости реакции по данному веществу i имеет вид (моль/м3 *с).
![]() (1.3.2)
(1.3.2)
dni – изменение количества i-того компонента, моль; S- площадь, м2;
dt – изменение времени, с.
I. Продукты реакции или промежуточные соединения образуются при взаимодействии частиц в элементарном химическом акте. Число частиц в элементарном химическом акте называется молекулярностью реакции. Элементарные реакции бывают трех типов:
- мономолекулярные А ® Р1+ Р2 + …
- бимолекулярные А + В ® Р1+ Р2 +...
- тримолекулярные 2А + В ® Р1+ Р2 + … 3А ® Р1+ Р2 + …,
А + В + С ® Р1+ Р2 + …
Четырехмолекулярных реакций не бывает, т.к. вероятность одновременного столкновения четырех молекул ничтожно мала.
Скорость реакции можно измерить, определяя количество реагента или продукта во времени. Скорость реакции зависит от природы реагирующих веществ и от условий, в которых реакция протекает. Важнейшими из них являются концентрация, температура и присутствие катализатора.
Рассмотрим реакцию между веществами А и В, протекающую по схеме
аА + вВ + …. → сС + dD + …
Скорость реакции зависит от концентраций А и В, однако заранее нельзя утверждать, что она прямо пропорциональна концентрации того или другого. Зависимость скорости химической реакции от концентрации реагирующих веществ выражается основным законом химической кинетики — законом действующих масс: скорость элементарной химической реакции прямо пропорциональна произведению концентрации реагирующих веществ в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
Для элементарной реакции
n1А + n2В ® n3С + n4Е + …
w= ![]() или w = k [A]nA
[B]nВ. (1.3.3)
или w = k [A]nA
[B]nВ. (1.3.3)
Выражение такого типа называют кинетическим уравнением, где k - константа скорости (не зависит от концентрации реагирующих реагентов и времени); CA, CB – текущие концентрации реагирующих веществ; n1, n2 - некоторые числа, которые называются порядком реакции по веществам А и В соответственно. Порядок реакции совпадает со стехиометрическими показателями элементарной реакции. Порядок реакции n – сумма показателей кинетических степеней в химическом уравнении реакции. Сумма показателей степеней n1 + n2 = n называется общим порядком реакции. Для элементарной реакции общий порядок равен молекулярности, а порядок по веществам равны коэффициентам в уравнении реакции. Порядок реакции по i-тому компоненту не равен его стехиометрическому коэффициенту в химическом уравнении сложной реакции.
1. Реакции нулевого порядка. Скорость этих реакций не зависит от концентрации реагирующего вещества n=0. Из уравнений 1.3.1 и 1.3.3 получим следующее
w=k или ![]() . (1.3.4)
. (1.3.4)
Интегрируя выражение (1.3.4) получаем:
CA,t=CA,0 – k0t, k0t = CA,0 – CA,t (1.3.5)
Введем понятие время полупревращения t1/2 – это время, в течение которого превращается половина исходного вещества.
Для реакции нулевого порядка в уравнение 1.3.5
подставим ![]()
t1/2=![]()
2. Реакции первого порядка. Для реакции первого порядка n=1 типа
А ® Р1+ Р2 + …, скорость прямо пропорциональна концентрации вещества А:
w=![]() ;
; ![]()
lnCA,t = lnCA,0 – kt
С=СА,t=CA,0 e-kt
t1/2= ![]()
3. Реакции второго порядка. Для реакции второго порядка n=2 типа
А + В ® Р1+ Р2 +..., если СА,0=СВ,0 кинетическое уравнение имеет вид
w=![]() ;
; ![]()
![]()
t1/2![]()
![]()
Для реакции второго порядка типа А + В ® Р + … если СА,0 ¹ СВ,0 кинетическое уравнение имеет вид
w=![]()
Периоды полураспада вещества А и В, если СА,0 ¹ СВ,0, различны,
т.е. t1|2 (A)¹ t1|2 (B).
4. Реакции третьего порядка. Кинетика реакции третьего порядка n=3 типа
2А + В ® Р1+ Р2 + … 3А ® Р1+ Р2 + …, А + В + С ® Р1+ Р2 + …
при равных начальных концентрациях описывается уравнением
w=![]()
t1|2=![]()
Для реакции А + В + С ® Р + …,если СА,0 ¹ СВ,0¹СС,0 кинетическое уравнение примет вид
w=![]()
II. Выражение (1.3.1) записано для фиксированной температуры. Для приближенной оценки изменения скорости широко используется эмпирическое правило Вант-Гоффа, в соответствии с которым скорость химической реакции становится в 2-4 раза больше при повышении температуры на каждые 10°C. В математической форме зависимость изменения скорости реакции от температуры выражается уравнением
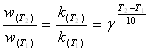 (1.3.4)
(1.3.4)
![]() — скорость реакции при
повышенной температуре Т2,
— скорость реакции при
повышенной температуре Т2,
![]() - скорость реакции при
начальной температуре Т1; γ —температурный коэффициент
скорости, показывающий, во сколько раз увеличится скорость реакции при
повышении температуры на 10°С (2-4). Это позволяет предположить, что между
скоростью реакции и температурой должна существовать экспоненциальная зависимость.
Точное соотношение между скоростью реакции и температурой установил шведский
химик Аррениус в 1899 г. Это соотношение, получившее название уравнение Аррениуса,
имеет вид
- скорость реакции при
начальной температуре Т1; γ —температурный коэффициент
скорости, показывающий, во сколько раз увеличится скорость реакции при
повышении температуры на 10°С (2-4). Это позволяет предположить, что между
скоростью реакции и температурой должна существовать экспоненциальная зависимость.
Точное соотношение между скоростью реакции и температурой установил шведский
химик Аррениус в 1899 г. Это соотношение, получившее название уравнение Аррениуса,
имеет вид
![]() (1.3.5)
(1.3.5)
где k – константа скорости реакции; А — постоянная, характеризующая каждую конкретную реакцию (константа Аррениуса, или «предэкспонента»);
Еa — постоянная, характерная для каждой реакции и называемая энергией активации, Дж; R — универсальная газовая постоянная Дж/(К*моль);
Т — температура, К.
Подчеркнем, что это уравнение связывает температуру не со скоростью реакции, а с константой скорости. Приведем уравнение Аррениуса для двух температур
![]()
III. Одно из наиболее сильных средств влияния на скорость реакции — присутствие в реагирующей системе катализатора - вещества, которое усиливают (а иногда и понижают - тогда его называют ингибитором) скорость химической реакции, но само не расходуется в этом процессе.
Примеры решения задач
1. Во сколько раз увеличится скорость химической реакции при повышении температуры с 0 до 50°С, принимая температурный коэффициент скорости равным трем?
Решение:
В математической форме зависимость изменения скорости реакции от температуры выражается уравнением
![]() =
=![]() γ
γ![]()
Температура увеличивается на 50°С, а γ = 3.
Подставляя эти значения, получим ![]() = 3
= 3![]() = 243
= 243
Ответ: скорость увеличится в 234 раза.
2. Для реакции первого порядка А→2В определите время за которое прореагировало на 90% вещества А. Константа скорости реакции 1*10-4 с-1.
Решение:
А → 2В
![]() ;
; ![]() ;
;
C0,A- CA=0,9 C0,A
CA = 0,1 C0,A
k1t = lnC0,A- lnCA
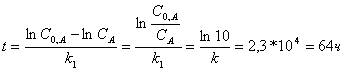 Ответ: 64 ч.
Ответ: 64 ч.
3. Как изменится скорость реакции 2А+В2
![]() 2АВ, протекающей и
закрытом сосуде, если увеличить давление в 4 раза?
2АВ, протекающей и
закрытом сосуде, если увеличить давление в 4 раза?
Решение:
По закону действия масс скорость химической
реакции прямо пропорциональна произведению молярных концентраций реагирующих
веществ: w=![]() . Увеличивая в сосуде
давление, мы тем самым увеличиваем концентрацию реагирующих веществ. Пусть начальные
концентрации А и В равнялись [А] =а,
. Увеличивая в сосуде
давление, мы тем самым увеличиваем концентрацию реагирующих веществ. Пусть начальные
концентрации А и В равнялись [А] =а,
[В]=b. Тогда w=ka2b. Вследствие увеличения давления в 4 раза увеличились концентрации каждого из реагентов тоже в 4 раза и стали [A]=4a, [B]=4b.
При этих концентрациях w1 =k(4а)2 *4b = k64а2b. Значение k и обоих случаях одно и то же. Константа скорости для данной реакции есть величина постоянная, численно равная скорости реакции при молярных концентрациях реагирующих веществ, равных 1. Сравнивая w и w1, видим, что скорость реакции возросла в 64 раза. Ответ: скорость реакции возросла в 64 раза.
4. Энергия активации некоторой реакции в отсутствие катализатора равна
76 кДж/моль и при температуре 27°С протекает с некоторой скоростью k1. В присутствии катализатора при этой же температуре скорость реакции увеличивается в 3,38 • 104 раз. Определите энергию активации реакции в присутствии катализатора.
Решение:
Константа скорости реакции в отсутствие катализатора запишется в виде
![]() = Ае
= Ае ![]() = Ae-30,485.
= Ae-30,485.
Константа скорости реакции в присутствии катализатора равна
![]() = Ае
= Ае ![]() = Ае
= Ае![]() .
.
По условию задачи
![]() =e – (- 30,485-
=e – (- 30,485-![]() )=3,38
* 104.
)=3,38
* 104.
Логарифмируем последнее уравнение и получаем
30,485 -![]() = 1n(3,38*104) =
10,43.
= 1n(3,38*104) =
10,43.
Отсюда Еа = 2493 • 20,057 = 50 кДж/моль.
Ответ: энергия активации реакции в присутствии катализатора равна 50 кДж/моль.
Задачи для самостоятельного решения
1. За какое время пройдет реакция при 60◦С, если при 20◦С она заканчивается за
40 с, а энергия активации 125,5 кДж/моль?
2. В загрязненном воздухе содержится примесь монооксида углерода, который образуется при неполном сгорании твердого топлива и работе двигателей внутреннего сгорания. Монооксид углерода медленно окисляется кислородом воздуха до диоксида углерода. Допустим, что при определенных условиях скорость такой реакции составляет 0,05 моль/л*с, а концентрация диоксида углерода равна 0,2 моль/л*с. Рассчитайте концентрацию диоксида углерода через 10 с после указанного момента.
3. Один из важных видов сырья для органического синтеза — так называемый водяной газ, представляющий собой смесь водорода и монооксида углерода. Эту смесь получают при пропускании водяного пара через башни, наполненные раскаленным углем. Из водяного газа получают метанол, формальдегид и другие вещества. Рассчитайте значение константы скорости реакции получения водяного газа, если при концентрации водяного пара, равной 0,03 моль/л скорость реакции составляет 6,1 • 10 -5 моль/л*с.
4. В реакции А + В → С с общим порядок равным 1, k1 = 5*10-5 c-1 Определите концентрации веществ А и В и скорость через 1 час и через 5 ч, если начальная концентрации А составляет 0,2 моль/л.
5. Причиной появления опасного для здоровья тумана (смога) считают образование большого количества выхлопных газов автомобилей при высокой влажности воздуха. В смоге присутствует ядовитый диоксид азота, который получается при реакции монооксида азота с атомарным кислородом. Рассчитайте скорость этой реакции, если через 5 мин после начала наблюдений концентрация диоксида азота была равна 0,05 моль/л, а через 20 мин - 0,08 моль/л.
6. Уравнение реакции омыления уксусноэтилового эфира:
СН2СООС2Н5 + NаОН = СН3СООNa+ С2Н5ОН
Исходные концентрации реагирующих веществ до начала реакции были: [СН3СООС2Н5] =0,50 моль/л, [NаОН] = 0,25 моль/л. Определить, как и во сколько раз изменится скорость реакции в момент, когда концентрация [СН3СООС2Н5] стала равной 0,30 моль/л.
7. Атмосферные загрязнения, например фторированные и хлорированные углеводороды — фреоны (СС13F, СС12F2, СС1F3), разрушают защитный озоновый слой Земли. Фреоны химически стабильны в нижних слоях атмосферы, но в стратосфере под действием ультрафиолетового излучения Солнца разлагаются, выделяя атомарный хлор, который и взаимодействует с озоном. Рассчитайте скорость такой реакции с образованием кислорода и монооксида хлора, если через 15 с после начала реакции молярная концентрация озона была 0,30 моль/л, а через 35с (от начала реакции) стала равна 0,15 моль/л.
8. За реакцией дегидрирования бутана, протекающей по уравнению
С4Н10 → С4Н8 + Н2 при температуре 800 К, следили по объему реагирующих газов, занимаемому ими при давлении 101 кПа и 293 К. Объем реактора 0,2 л, скорость протекания реакции равна 1,33 • 10-2 кПа/с. Рассчитайте, через какое время после начала реакции изменение объема достигнет 0,01 л.
9. Рассчитайте изменения константы скорости реакции, имеющей энергию активации 191 кДж/моль, при увеличении температуры от 330 до 400 К.
10. Вычислите порядок реакции и константу скорости, если при изменении начальной концентрации с 0,502 моль/л до 1,007 моль/л время полупревращения уменьшится с 51 с до 26 с.
11. Для реакции омыления уксусно-этилового эфира при большом избытке воды константа скорости при 20ºС равна 0,00099 мин-1, а при 40С ее величина составляет 0,00439 мин-1. Определите энергию активации и константу скорости реакции при 30ºС.
3.2 Технико-экономические показатели химических производств
Значение химии становится особенно ясным, когда изучаемый материал связывается с практическими вопросами. Один из способов его связи с жизнью — решение задач на темы с производственны содержанием. Для химической промышленности, как отрасли материального производства имеет значение технический и экономический аспекты, от которых зависит нормальное функционирование производства. Технико-экономические показатели (ТЭП) отражают возможности предприятия выпускать продукцию заданной номенклатуры и качества, удовлетворяющий требованиям заказчика, и в заданном количестве. Они являются критериями, позволяющий установить экономическую целесообразность организации данного производства и его рентабельность.
Рентабельность процесса производства характеризуется следующими ТЭП: степень превращения, выход продукта, селективность, производительность, мощность и интенсивность аппаратуры, практический и теоретический расходный коэффициент.
В этом разделе рассматриваются задачи следующих типов:
1. Задачи, в которых обращается внимание на получение вещества или на применение его в производственных условиях.
2. Задачи на определение выхода получаемого вещества по отношению к теоретическому.
3. Задачи, вскрывающие химическую сторону технологии производства и требующие составления уравнения реакции по которой оно протекает.
4. Задачи, в которых обращается внимание на масштабы производства или размеры аппаратуры (башен, камер, колонок) и т. п.
Степень превращения (![]() ) – это отношение
количества вещества, вступившего в реакцию, к его исходному количеству
вещества. Допустим, протекает простая необратимая реакция типа А → В.
Если обозначить через
) – это отношение
количества вещества, вступившего в реакцию, к его исходному количеству
вещества. Допустим, протекает простая необратимая реакция типа А → В.
Если обозначить через ![]() исходное
количество вещества А, а через
исходное
количество вещества А, а через ![]() -
количество вещества А в данный момент, то степень превращения реагента А
составит
-
количество вещества А в данный момент, то степень превращения реагента А
составит
![]() (2.1)
(2.1)
Чем выше степень превращения, тем большая часть исходного сырья вступила в реакцию и полнее прошел процесс химического превращения.
Выход продукта (η) является показателем совершенства процесса и показывает отношение количества фактически полученного количества того или иного продукта к его теоретическому количеству.
![]() ;
; ![]() (2.2), (2.3)
(2.2), (2.3)
Производительность аппарата (П) определяет количество готового продукта m фактически вырабатываемый в единицу времени t при заданных условиях процесса производства. Измеряется т/сут, тыс.т/год, кг/ч, нм3/сут.
![]() (2.4)
(2.4)
Интенсивность аппарата – производительность, отнесенная к единице полезного объема или к единице полезной площади. Измеряется кг/м3 и кг/м2
![]() или
или ![]() (2.5), (2.6)
(2.5), (2.6)
Максимально возможная производительность аппарата при оптимальных условиях процесса производства называется его мощностью W
W=Пmax (2.7)
Селективность – отношение массы целевого продукта к общей массе продуктов, полученных в данном процессе, или к массе превращенного сырья за время t.
Если А → В, А → С, где В – целевой продукт, С – побочный продукт, то уравнение имеет следующий вид:
![]() (2.8)
(2.8)
Это отношение скорости превращения вещества А в целевой продукт к общей скорости расхода вещества А.
![]()
Расходный коэффициент Кр определяет расходы сырья, воды, топлива, электроэнергии пара на единицу произведенной продукции
![]() (2.9)
(2.9)
Gисх – затраты сырья, топлива, энергии при производстве продукта в количестве G. Измеряется в т/т, нм3/т, нм3/ нм3, кВт*ч/т.
Примеры решения задач
1. Сколько теоретически можно получить чугуна, содержащего 3% углерода и 3% других элементов, из 1 т железной руды, содержащей 80% железа?
Из каждой тонны железной руды, содержащей в среднем 80% магнитного железняка, выплавляют 570 кг чугуна, содержащего 95% железа. Каков был выход железа от теоретического?
Решение:
М(Fе3О4) = 232 г/моль
М(Fе) = 56 г/моль
Записываем формулу определения η(Fе):
![]()
Обеих величин в условии нет. Но m(Fе)пр можно рассчитать по массе чугуна и массовой доле железа в нем:
m(Fе)пр = 570 кг • 0,95 = 541,5 кг.
Сразу теоретическую массу железа по условию не вычислить. Можно найти массу магнитного железняка по массе руды и содержанию в ней массовой доли железняка:
m(Fе3О4) = 1000 кг • 0,8 = 800 кг.
По вычисленной массе магнитного железняка и его формуле найдем массу железа в нем:
800 > 232 в 3,45 раза => m(Fе) будет > 168 (56 • 3) тоже в 3,45 раза, т. е.
M(Fе) = 168 • 3,45 = 579,6 (кг).
Подставляя полученные значения практической и теоретической массы железа в первоначальную формулу, получим выход железа:
η(Fе) = ![]()
Ответ: η(Fе) =93,4%.
2. Для получения формальдегида метиловый спирт необходимо окислить на серебряном катализаторе: СН3ОН + 0,5О2 = СН2О + Н2О. Кроме основных реакций протекают и побочные. Предположим, что на окисление подается 3,2 кмоль метилового спирта. Их них образовалось 1,8 кмоль формальдегида, 0,8 моль – побочных продуктов (суммарно) и остались неокисленными 0,6 кмоль метилового спирта. Необходимо найти степень превращения метилового спирта, выход формальдегида и селективность.
Решение:
Определим степень превращения. Для этого количество непрореагировавшего спирта, оставшегося после реакции, 0,6 кмоль необходимо вычесть из его начального количества 3,2 кмоль. Подставив данные значения в формулу (2.1) получим:
![]()
Рассчитаем селективность по формальдегиду. Общее количество полученных продуктов равно сумме количества формальдегида 1,8 кмоль и количества продуктов 0,8 кмоль.
![]()
Найдем выход продукта формальдегида.
![]()
Ответ: ![]() = 0,81, φ(НСНО)=
0,69, η(НСНО)= 56%
= 0,81, φ(НСНО)=
0,69, η(НСНО)= 56%
Задачи для самостоятельного решения
1. Рассчитать основные технико-экономические показатели получения синтетического аммиака:
а) расходный коэффициент сырья по Н2 и N2 (в м3) на 1т аммиака.
Б) выход аммиака
в) производительность завода.
Г) интенсивность процесса синтеза аммиака в т/м3 полезного объема колонки в сутки. На 1т аммиака практически расходуется 3000 нм3 азотоводородной смеси, теоретически 2635 нм3. 5 колонок с высотой 0,36 м.
2. Вычислить расходный коэффициент на 1т СН3СООН для СаС2, содержит 65% СаС2, если выход С2Н2 97%, уксусного альдегида 95% и СН3СООН 96%.
3. Вычислить количество аммиака и СО2 (в кг) израсходованных на производство мочевины. Потери мочевины 5% избыток аммиака 100%, степень превращения карбомата аммония мочевину 75%
4. При окислительном дегидрировании метилового спирта протекают одновременно две реакции: дегидрирование и окисление метанола. Выход формальдегида 90% при степени конверсии метанола 65%. Вычислите расход метанола на 1т формальдегида.
5. Производительность мечи для обжига серного колчедана составляет 30т в сутки. Выход SО2- 97,4% от теоретического. Сколько тонн SО2 производит печь в сутки, если содержание серы в колчедане 42,4%?
6. Печь для варки стекла, производящая в сутки 300т стекломассы имеет ванну длиной 60м, шириной 10м и глубиной 1,5 м. Определить:
а) годовую производительность, если 15 суток печь находится на ремонте
б) интенсивность печи за сутки работы.
В) количество листов оконного стекла за из свариваемой стекломассы (стандарт. Лист 1250 * 700 * 2 мм и плотность 2500 г/м3)
7. При прямой гидратации этилена наряду с основной реакцией присоединения Н2О протекают побочные реакции. Так 2% (от массы) этилена расходуется на образование простого диэтилового эфира, 1% ацетальдегида, 2% низкомолекулярного жидкого полимера. Общий выход спирта при многократной циркуляции сост. 95%. Напишите уравнению химической реакции образовавшихся выше перечисленных соединений и подсчитайте расход этилена на 1т этилового спирта, и сколько диэтилового эфира может при этом получится.
8. Шахтная печь для получения оксида кальция имеет в среднем высоту
14 м и диаметр 4 м; выход оксида кальция составляет 600- 800 кг на 1 м3 печи в сутки. Определите суточный выход оксида кальция.
9. Производительность печи для обжига колчедана составляет 30 т колчедана в сутки. Колчедан содержит 42,2% серы. Воздух расходуется на 60% больше теоретического. Выход сернистого газа составляет 97,4%.
Вычислить а) содержание колчедана FеS2 (в%); б) объем и состав газовой смеси, выходящей из смеси за 1 час; в) массу оставшегося в печи огарка; г) массу оставшегося в печи не прореагировавшего FeS2.
10. Протекают две параллельные реакции 2А → С и А → 3В. Определите выход продукта С, степень превращения реагента А и селективность по продукту В, если на выходе из реактора известно количество веществ ν(А) = 2 моль, ν(С)=ν(В)=3 моль.
3.3 Задачи с экологическим содержанием
Охрана воздушного и водного бассейнов, защиты почв, сохранение и воспроизводство флоты и фауны – важные проблемы современности. В нашей стране разработано несколько общих направлений защиты биосферы от промышленных выбросов: создание безотходных технологий, замкнутых систем производств, основанный на полном комплексном использовании сырья; уменьшение объема промышленных стоков путем создания бессточных производств; проведение мероприятий по уменьшению загрязнения биосферы газообразными выбросами сжигания топлива; разработка методов утилизации; и обезвреживания производственных отходов и выбросов на действующих предприятиях.
Экологическая химия – наука, изучающая основы экологических явлений и химических процессов, происходящих в природе. В данном разделе применяются основные законы и формулы, применяемые для расчета массы, количества вещества, объема, концентрации, в том числе и для определения предельно-допустимых концентраций.
Предельно-допустимая концентрация (ПДК) – это такая концентрация, которая не оказывает на живые организмы прямого или косвенного влияния, не снижает его работоспособность, самочувствие. Основной задачей газоочистки и очистки сточных вод служит доведение содержания токсичных примесей в газах и сливных водах до ПДК установленных санитарными нормами. При невозможности достигнуть ПДК путем очистки иногда применяют многократное разбавление токсичных веществ или выброс газов через высокие дымовые трубы для рассеивания примесей в верхних слоях атмосферы. Для санитарной оценки среды используют несколько видов ПДК.
- ПДК воздушной среды;
- ПДК водной среды;
- ПДК почвы.
Для определения предельно-допустимой концентрации применяют следующую формулу:
![]() ,
,
где Сm – предельно-допустимая концентрация, m – масса токсичного соединения,
V – объем, в котором присутствует соединение данной массы.
Теоретическое определение концентрации примесей в нижних слоях атмосферы в зависит от высоты трубы. Высота трубы, от которой зависит содержание примесей в приземном слое воздуха, рассчитывается по эмпирической формуле:
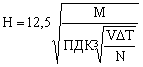
![]()
где М – количество вредных веществ, выбрасываемых в атмосферу, г/с; V – объем выбрасываемых газов, м3 /с; ∆Т – разность между температурами выходящих газов и окружающего воздуха, ◦С; N – число труб, через которые выводятся отходные газы.
Предельно допустимый выброс (ПВД) вредных примесей в атмосферу, обеспечивающий концентрацию этих веществ в приземном слое воздуха не выше ПДК, рассчитывается по формуле
![]()
где А – коэффициент, определяющий условия вертикального и горизонтального рассеивания вредных веществ в воздухе; F- коэффициент, учитывающий скорость седиментации вредных веществ в атмосфере; m- коэффициент, учитывающий условия выхода газа из устья трубы. Коэффициент m может быть вычислен по формуле
![]()
где v –средняя скорость газа на выходе из трубы, м/с; d - диаметр трубы, м.
Примеры решения задач.
1. В настоящее время муравьиную кислоту получают из природного газа путем каталитического окисления содержащегося в нем метана. Вычислите объем природного газа (и. у.), необходимого для получения муравьиной кислоты массой 69 т, если объемная доля метана в нем равна 0,95. Определите преимущества данной технологии по сравнению с методом получения муравьиной кислоты путем разложения формиата натрия серной кислотой при охлаждении раствора.
Решение:
СН4 + 3[О] →НСООН+Н2О
ν(НСООН) =![]() =
=![]() =1,5*106 моль;
=1,5*106 моль;
V(СН4) =ν*Vm= 1,5*106 моль*22,4 л/моль=33,6*105 л.
V(природного газа)=33,6* 106 л: 0,95=35,37*106 л=35,37*103 м3
Ответ: объем природного газа равен 35,37*103 м3.
Современный способ получения муравьиной кислоты дает экономическую выгоду, так как его использование уменьшает расход ценного сырья. Экологическая выгода заключается в том, что если природный газ используют без предварительной переработки, то это вызывает попадание в атмосферу большого количества продуктов его сгорания: оксидов серы, азота, углерода, которые загрязняют окружающую среду. Данная технология получения муравьиной кислоты имеет также преимущества в сравнении с синтезом кислоты из формиата натрия, который осуществляется в несколько стадий и дает в качестве побочных продуктов производства соли серной кислоты, кислотные и щелочные сточные воды.
Природный газ данного объема почти полностью расходуется на получение муравьиной кислоты. Следовательно, выброс отходов производства в окружающую среду уменьшается по сравнению с методом получения ее разложением формиата натрия, так как используется малоотходная технология.
2. В сточных водах химико-фармацевтического комбината был обнаружен хлорид ртути HgCl2, концентрация которого составила 5 мг/л. Для его очистки решили применить метод осаждения. В качестве осадителя использовали сульфид натрия (Na2S) массой 420 г. Будут ли достаточно очищены сточные воды, чтобы допустить их сброс в соседний водоем, содержащий 10 000 м3 воды?
ПДК (HgCl2) = 0,0001 мг/л. Объем сточных вод 300 м3
Решение:
HgCl2 + Na2S = HgS + 2NaCI
C(HgCI2)= 5 мг/л = 5 * 10-3г/л; V=300 м3 = 300*10 3л;
m(HgCl2)=1500г
ν(HgCl2)= 5,52 моль
m(Na2S) =420 г; ν(Na2S) = 5,38 моль. Согласно уравнения реакции в недостатке содержится сульфид натрия, в избытке - хлорид ртути. Останется хлорида ртути количеством 0,14 моль, m =0,14 моль*271,58 г/моль= 38 г.
m (HgCl2) = 38 г;
Находим ПДК
![]()
Это число значительно превышает ПДК. Однако при
сбросе сточных вод в природный водоем концентрация хлорида ртути понизится и будет
равна: ![]() . Полученное число также
больше ПДК. Таким образом, сброс воды недопустим.
. Полученное число также
больше ПДК. Таким образом, сброс воды недопустим.
Ответ: Сm (HgCl) = 0,127 мг/л в сточных водах и 0,0037 мг/л в открытом водоеме, что значительно больше ПДК.
3. Как можно утилизировать доменный газ?
Решение:
Доменный газ имеет высокую температуру, поэтому на первой стадий его
переработки осуществляют утилизацию тепла, на второй - от газа отделяют
колошниковую пыль (оксиды меди) с помощью циклонов и электрофильтров. В дальнейшем доменный газ используют в качестве топлива. Кроме того, его
можно очистить от оксидов серы по реакции Клауса:
SO2 + 2H2S = 3S + 2Н2О.
Следует отметить, что в настоящее время доменный процесс считается бесперспективным. Его заменяют прямым восстановлением железа из руды.
Задачи для самостоятельной работы
1. В радиусе 2 км вокруг химического завода ощущается легкий запах сероводорода. Анализ проб воздуха, отобранных с вертолета, показал, что газ находится в атмосфере на высоте до 2,0 км. Средняя концентрация сероводорода в воздухе составляет 1/20 промышленно допустимой концентрации (ПДК), равной 0,01 мл/л. Сколько тонн серной кислоты (считая на безводную) можно было бы получить, если бы удалось уловить весь сероводород в этом пространстве?
2. Картофель, выращенный вблизи шоссе, всегда содержит весьма ядовитые соединения свинца. В пересчете на металл в 1кг такого картофеля было обнаружено 0,001 моль свинца. Определите, во сколько раз превышено предельно допустимое содержание свинца в овощах, значение которого равно 0,5 кг?
3. Природный газ содержит главным образом метан СН4, но в нем присутствуют и примеси, например ядовитый сероводород Н2S — до 50 г на 1 кг метана. Чтобы удалить примесь сероводорода, можно окислить его перманганатом калия КМnО4 в кислой среде до серы. Рассчитайте массу серы, которую можно таким образом выделить из 1 т природного газа. Определите также массу серной кислоты, которая может быть получена из этой серы.
4. Диоксид серы образуется в основном при сжигании твердого топлива на тепловых электростанциях. Это бесцветный газ с резким запахом, он сильно раздражает слизистые оболочки глаз и дыхательных путей. Наличие диоксида серы в атмосфере — причина кислотных дождей, поскольку под действием кислорода воздуха и воды диоксид серы превращается в серную кислоту. Однако далеко не все производства, в выбросах которых содержится диоксид серы, имеют современные сооружения для газоочистки. Чаще применяется разбавление выбросов чистым воздухом или рассеивание их в воздушной среде путем устройства дымовых труб большой высоты. Установлено, что при высоте трубы 100 м на расстоянии 2 км от предприятия содержание диоксида серы в воздухе равно 2,75 мг/м3. Во сколько раз этот показатель превышает значение предельно допустимой концентрации, равное 7,8*10-6 моль/м3.
5. Формальдегид НСНО применяется при изготовлении древесностружечных плит, красок, искусственного волокна, лекарственных средств, оргстекла и т.п. Он обладает сильным и резким запахом и угнетающе действует на сердечнососудистую и нервную системы. Запах формальдегида чувствуется при его содержании в воздухе, равном 0,2 мг/м3, а санитарные нормы требуют, чтобы примесь формальдегида в воздухе не превышала 0,003 мг/м3. Рассчитайте молярную концентрацию формальдегида: а) при полном соответствии воздуха санитарным нормам; б) при появлении запаха формальдегида.
6. Рассчитайте, какой высоты должна быть труба, чтобы концентрация оксида серы (IV) в приземистом слое воздуха не превышала ПДК (0,5 мг/г3). Отходящий топливный газ с объемной долей оксида серы (IV) 0,05% поступает в дымовую трубу со скоростью 300 м3/ч при температуре 130◦С. Температура воздуха 20◦С.
7. Незаконное захоронение ртути привело к тому, что ее содержание в 1кг почвы на некотором участке лесопарковой зоны составило 0,005 моль. ПДК ртути в почве равно 21 мг/кг. Во сколько раз превышено значение ПДК ртути в почве?
8. Водный раствор 0,001 моль йода в избытке йодида калия полностью обесцветился после пропускания через него 1м3 воздуха. Рассчитайте содержание диоксида серы (мг/м3) в исследуемом воздухе и сравните полученный результат с ПДК (SO2), равной 0,05мг/м3. Превышено ли значение ПДК диоксида серы?
9. Историки полагают, что случаи отравления соединениями свинца в Древнем Риме были обусловлены использованием свинцовых водопроводных труб. Свинец в присутствии диоксида углерода взаимодействует с водой. При этом образуется растворимый гидрокарбонат свинца:
Рb+СО2+Н2О=РbСО3+Н2↑
РbСО3+СО2+Н2О=Рb(НСО3)2
Катионы свинца не приносят вреда здоровью, если их содержание в воде не превышает 0,03 мг/л. Во сколько раз оно было превышено, если считать, что 1 литр водопроводной воды содержал 0,0000145 моль Рb2+?
10. При производстве серы автоклавным методом неизбежно выделяется около
3 кг сероводорода на каждую тонну получаемой серы. Сероводород — чрезвычайно ядовитый газ, вызывающий головокружение, тошноту и рвоту, а при вдыхании в большом количестве - поражение мышцы сердца и судороги, вплоть до смертельного исхода. Какой объем сероводорода (при н. у.) необходимо поглотить в системах газоочистки при получении 125 т серы на химзаводе?
11. На нефтеперерабатывающем заводе из-за поломки произошел аварийный выброс нефтепродуктов в ближайшее озеро. Масса сброшенных продуктов составила 500 кг. Выживут ли рыбы, обитающие в озере, если известно, что примерная масса воды в озере 10000 т. Токсичная концентрация нефтепродуктов для рыб составляет 0,05 мг/л.
12. Определите ПВД фтороводорода (в г в сек), обеспечивающий концентрацию его в приземном слое атмосферы в районе суперфосфатного завода не выше ПДК 0,05 мг/м3, при высоте дымовой трубы 100 м и ее диаметре 0,7 м. Объем газового выброса равен 160, а коэффициент седиментации – 1. Средняя скорость газа на выходе из трубы – 0,4 м/с. Температура выходящего газа 40С, а атмосферы – 23С.
3.4 Производство неорганических соединений
3.4.1 Металлургия
Металлургия – это наука о промышленных способах получения металлов из природного сырья. Металлургией также называю металлургическую промышленность. Сырьем в производстве металлов является металлические руды. За исключением небольшого числа металлов находящихся в природе в виде химических соединений входящих в состав металлических руд. Основной задачей металлургической промышленности является получение металлов из руд. Для этого руду подготавливают, подвергают вторичной обработке и процессу восстановления.
Задачи, которые приводятся в этом разделе являются расчетными задачами по уравнениям химических реакций. При решении задач используют основные законы и формулы химии, а также формулы которые рассматривались в предыдущих разделах (выход продукта, интенсивность, производительность и тд.)
Одной из важнейших задач химической технологии является обогащение сырья. Для этого применяют метод флотации, который основан на различной смачиваемости водой минералов.
Выход концентрата (Вк) называется процентное отношение веса полученного концентрата к весу взятой руды.
Степень извлечения (Си) называется процентное отношение веса извлеченного элемента в концентрате к его весу в руде.
Степенью обогащения (Со) называется отношение процентного содержания элемента в концентрате к содержанию его в исходной руде.
В этом разделе при решение задач используют следующие понятия: выход продукта, расчет состава руды, возможность самопроизвольного протекания реакции получения металла, которые подробно описываются в других разделах.
Примеры решения задач
1. Рассчитать минимальный расход магния для удаления сурьмы из 10 т чернового свинца, в котором сурьма составляет 0,5% массы. Сурьма выделяется из сплава в составе соединения Мg3Sb2
Решение:
Составим первое уравнение масса магния, добавленного в черновой сплав, равна массе магния в выделившемся из сплава соединении Mg3Sb2. Запишем второе уравнение, полагая, что масса сурьмы, содержащейся в 10 т чернового сплава, равна массе сурьмы и образовавшемся соединении Мg3Sb2.
![]() m(Mg) =
m(Mg) =![]() m(Mg3Sb2)*(3*M(Mg)/M(Mg3Sb2)
m(Mg3Sb2)*(3*M(Mg)/M(Mg3Sb2)
10*0,005 = m(Mg3Sb2)*(2*M(Sb)/M(Mg3Sb2)
Или
![]() m(Mg) = m(Mg3Sb2)*(3*24)/316
m(Mg) = m(Mg3Sb2)*(3*24)/316
0,05 = m(Mg3Sb2)*(2*122/316)
Для решения системы уравнении разделим правую и левую части первого уравнения на соответствующие части второго и обозначая (Мg) через х, получим:
x/0,05=24*3/122*2, x=0,0148
Ответ. Минимальный расход магния— 14,8 кг.
2. На обогатительной фабрике флотации подвергается руда, содержащая 1,3% меди. При флотации 1т исходной руды получится 110,5 кг концентрата, содержащего 9,6% меди. Определите выход концентрата, степень извлечения и степень обогащения.
Решение
1.Вк= ![]()
2. Для вычисления Си рассуждаем так
а) в 100 кг исходной руды содержится 1,3 кг меди
в 1000 кг ---------------------------------- х кг меди
х= 13 кг меди
б) в 100 кг концентрата содержится 9,6 кг меди
в 110,5 кг ---------------------------------- х кг меди
х= 10,6 кг меди.
Следовательно, степень извлечения будет равна
Си=![]()
3. Со=![]() раза.
раза.
Ответ Вк=11,05%, Си=81,5%, Со=7,4 раза.
Примеры решения задач
1. Имеется титановая руда, состоящая из минералов рутила, перовскита и пустой породы. Массовая доля ТiО2 в этих минералах составляет соответственно 97% и 59%. Вычислить массовые доли названных выше минералов в руде, если известно, что содержание титана равно 27% от массы руды, а пустой породы – 38%.
2. Для легирования стали, требуется внести в расплав титан, чтобы его массовая доля составила 0,12%. Какую массу сплава ферротитана надо добавить к расплаву стали массой 500 кг, если массовые доли металлов в ферротитане составляют: титана – 30%, железа – 70%
3. Некоторая порода состоит из минералов сильвинита (KCl), каинита (MgSO4*KCl*3H2О) и карналлита (MgCl2*KCl*6H2О). Массовая доля калия в породе составляет 18%, а примесей (не содержащих калия и магния) – 12%. Вычислите возможную массу магния в 100 кг породы.
4. При обогащение 10 т медной сульфидной руды, содержащей 1,5% меди, получено 400 кг концентрата, содержащего 30% меди. Определить степень извлечения и степень концентрации.
5. При флотации 5т цинковой руды, содержащего 3%
цинка, получено 340 кг концентрата, содержащего 22% цинка. Определите выход
концентрата, степень извлечения и степень концентрации. ![]()
6. Восстанавливая углем соединение Fe(CrO2)2 (хромистый железняк), получают сплав феррохром, используемый в металлургии. Определите массовую долю хрома в этом сплаве, считая, что других компонентов, кроме железа и хрома, он не содержит.
7. Железная руда имеет состав: магнетит Fе3О4 (массовая доля 55%), ильменит FеТiО3 (массовая доля 15%) и другие вещества, не содержащие железо и титан. Какую массу железа и титана можно получить из такой руды массой 300 кг?
8. Из медной руды массой 16т, содержащей халькозин Cu2S и вещества, не содержащие медь, получили черновой металл массой 650 кг. Определите массовые доли меди и халькозина в руде, если массовая доля меди в черновом металле составляет 98,46%.
9. Для удаления висмута из черного свинца к расплавленному металлу добавляют сплав Pb – Ca, массовая доля кальция в котором составляет 0,03. Рассчитать теоретический расход сплава Pb – Ca для удаления висмута из 100 т чернового свинца, массовая доля висмута в котором равна 0,001. Висмут выделятся из сплава в составе соединения Ca3Bi2.
10. Медная руда содержит CuCO3*Cu(OH)2 и азурит 2CuCO3*Cu(OH)2 Какую массу меди можно получить из руды массой 5т, если массовая доля малахита 8%, азурита 3,6%. Определите массовую долю меди в руде.
3.4.2 Электрохимические производства
Электролизом называется окислительно-восстановительная реакция, протекающая при пропускании постоянного электрического тока через расплав или раствор электролита.
Сущность электролиза заключается в следующем: при пропускании электрического тока через расплав или раствор электролита положительные ионы электролита (ионы металлов или водорода) притягиваются катодом, а отрицательные ионы (кислотные остатки или гидроксильные группы) — анодом. Приносимые к катоду от источника тока электроны присоединяются к положительным ионам электролита, восстанавливая их. Одновременно отрицательные ионы электролита отдают свои электроны аноду, от которого они двигаются к источнику тока. Теряя свои электроны, они окисляются в нейтральные атомы или группы атомов. Таким образом, у катода протекает процесс восстановления, а у анода — процесс окисления.
А (+): nAn- - ne- → nAp-
K (-): nBn+ + ne- → nBp+
Оба процесса образуют единую окислительно-восстановительную реакцию. Но в отличие от обычных окислительно-восстановительных реакций электроны от восстановителя к окислителю переходят не прямо, а посредством электрического тока. Катод, приносящий электроны, является восстановителем, а анод, уносящий их,— окислителем.
Основными показателями электрохимических производств являются выход по току, степень использования энергии. Расходный коэффициент по энергии, напряжение, приложенное к электролизеру, и др. Большинство вычислений основано на законе Фарадея, согласно которому масса вещества, выделившегося при электролизе пропорционально силе тока I, времени электролиза t и электрохимическому эквиваленту этого вещества ЭЭ
Масса вещества вычисляется по формуле
![]() (1.3.1)
(1.3.1)
где, I - сила тока, F – постоянная Фарадея (96500 Кл)
![]() (г-экв) (1.3.2)
(г-экв) (1.3.2)
Mr – относительная молекулярная масса вещества,
n – заряд иона (абсолютное значение) в виде которого вещество находится в растворе или в расплаве (т.е. количество отданных или принятых электронов).
Выход по току определяется отношением массы вещества, выделившегося при электролизе, к массе вещества, которое теоретически должно выделится согласно закону Фарадея, и выражается в процентах:
![]() (1.3.3)
(1.3.3)
Масса mтеор находится по формуле
![]()
![]() (1.3.4)
(1.3.4)
Выход по энергии определяется по уравнению
![]() (1.3.5)
(1.3.5)
где, Етеор и Епр – теоретическое и практическое напряжение разложения при электролизе соответственно, В; η - выход по энергии,%.
Выход по энергии может быть вычислен и по количеству затраченной энергии:
![]() (1.3.6)
(1.3.6)
где wтеор и wпр – количество энергии, теоретически необходимое и практически затраченное на получение единицы продукта.
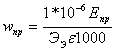 (1.3.7)
(1.3.7)
где 1000 – коэффициент перевода Вт*ч в кВт*ч;
1*10-6 – число, используемое для перевода граммов в тонны.
Теоретический расход электроэнергии находится по отношению
![]() (1.3.8)
(1.3.8)
где φразл – напряжение разложения.
Примеры решения задач
1. Какие процессы происходят при электролизе расплава гидроокиси натрия?
Решение:
В расплаве едкого натра содержатся ионы Nа+
и ОН![]() .
Окисляющиеся у анода ионы ОН
.
Окисляющиеся у анода ионы ОН![]() в следующей стадии разлагаются с
образованием воды и кислорода. Процесс можно изобразить следующим образом:
в следующей стадии разлагаются с
образованием воды и кислорода. Процесс можно изобразить следующим образом:
К(-): 2Na+ + 2е- = 2Na;
А(+): 2ОН![]() - 2e- = Н2О
+ О2
- 2e- = Н2О
+ О2
Два атома кислорода, соединяясь друг с другом, образуют молекулу кислорода О2. Таким образом, суммарное уравнение
4NаОН = 4Na + 2Н2О + О2
При электролизе расплавов солей кислородных кислот окисляющиеся ионы кислотных остатков тут же разлагаются на кислород и соответствующие оксиды.
Своеобразно протекает электролиз в водном растворе. Дело в том, что сама вода — электролит, хотя и очень слабый. Таким образом, в водном растворе фактически содержатся два электролита — растворитель и растворенное вещество и соответственно по два вида как положительных, так и отрицательных ионов. Какие из них будут разряжаться, зависит от ряда условий. Как правило, можно руководствоваться следующим. Если положительные ионы электролита являются ионами очень активных металлов, как например Na+ или К-, то при электролизе разряжаются не ионы этих металлов, а ионы водорода из воды с выделением свободного водорода и освобождением гидроксильных ионов, что может быть выражено следующим электронно-ионным уравнением:
2H+OH![]() + 2е- = Н2↑
+ 2ОН
+ 2е- = Н2↑
+ 2ОН![]()
Если отрицательными ионами электролита являются
кислотные остатки кислородных кислот, то при электролизе разряжаются не
кислотные остатки этих кислот, а ионы ОН![]() из воды с выделением кислорода,
что можно выразить уравнением:
из воды с выделением кислорода,
что можно выразить уравнением:
4Н2О — 4е- = 4Н+
+ 4ОН![]()
4ОН- ![]() 2Н2О+О2
2Н2О+О2
Складывая оба уравнения, получаем:
2Н2О — 4е- = 4H+ + O2
2. Определить выход по току (в%), если в течение 24 ч в электролизере раствора поваренной соли при силе тока 15500А было получено 4200 л электролитической щелочи с концентрацией NaOH 125 кг/м3.
Решение:
По уравнению (1.3.4) масса гидроксида натрия теоретически должна была составить
![]()
практически было получено
![]()
Следовательно, выход по току по формуле (1.3.3) будет равен
![]()
Ответ: выход по току 94,6%.
3. Определите фактический расход электроэнергии (в киловатт-часах) на получение хлора массой 1 т и выход по энергии (в%), если среднее напряжение на электролизере 3,35В, выход по току 96%, а электрохимический эквивалент хлора равен 1,323 г/А*ч.
Решение:
Использовав формулу (1.3.7), определим фактический расход энергии
![]()
Если принять выход по току за 100%, то при теоретическом напряжении разложения NaCl, равном 2,17В, теоретический расход энергии на 1т хлора составит
![]()
В этом случае выход по энергии
![]()
Ответ: выход по энергии 62,2%; 2637 кВ/ч
Задачи для самостоятельного решения
1. Один из способов промышленного получения кальция – электролиз расплавленного хлорида кальция. Какая масса металла будет получена, если известно, что в результате электролиза выделился хлор объемом 896 л (н.у.)?
2. При электролизе раствора хлорида натрия в электролизе, работавшем в течении 24ч при силе тока 30000 А, было получено 8,5 м3 электролитической щелочи с концентрацией NaOH 120 кг/м3. рассчитать выход по току (для щелочи)
3. Определить силу тока, необходимые для выработки 100% -ного гидроксида натрия массой 1720 кг в сутки в электролизере с железным катом при его непрерывной работе, если выход по току составляет 96%
4. Вычислить массу хлора, вырабатываемого за год заводом, на котором установлено 5 серий по 150 электролизеров с железными катодами при непрерывной работе в течении 350 дней, силе тока 34000 А и выходе по току 95%. Определить мощность генератора переменного тока электростанции, обеспечивающий потребности завода в электрической энергии при напряжении донной серии 550 В, если КПД выпрямителя тока составляет 95%.
5. Вычислить теоретический и практический расход электроэнергии на 1т 100% NаОН для электролиза раствора хлорида натрия с ртутным катодом. Теоретическое напряжение разложения равно 3,168 В. Определить выход по энергии, если практическое напряжение разложения 4,4 В, а выход по току 92,5%.
6. Какие вещества, и в каком количестве выделяются на угольных электродах, если состав раствора 0,1 моль HgCl2 и 0,2 моль CuCl2 и через него пропускается ток силой 10 А в течение 1 ч?
7. При прохождении электрического тока через разбавленный раствор серной кислоты в течении 10 мин выделилось 100 мл водорода при 18С и давлении
755 мм рт. ст. Вычислите силу тока.
8. При электролитическом получении магния в качестве электролита может служит расплавленных хлорид магния. Вычислите выход по току, если в ванне, работающем при силе тока 40000 А, в течении 5 ч, выделилось 72,6 кг магния.
9. Определить количество электричества, необходимое для выделения 1 м3 водорода и 0,5 м3 кислорода, получаемое при электролизе воды. Теоретическое напряжение воды равно 1,23 В, а фактическое превышает его в 1,5 – 2 раза. Рассчитать фактический расход электрической энергии.
10. При электролизе раствора содержащего 2,895 г смеси FeCl2 и FeCl3, на катоде выделилось 1,12 г металла. Вычислите массовую долю каждого из компонентов исходной смеси, если электролиз проводили до полного осаждения железа.
3.5 Производство органических соединений
Основной или тяжелый органический синтез – это производство в больших количествах важнейших органических веществ преимущественно жирного ряда и простых по строению: спиртов (метилового, этилового), галогенопроизводных (винилхлорид), альдегидов и кетонов (формальдегид, ацетон), карбоновых кислот (муравьиная, уксусная, ВЖК), алкенов, диеновых УГВ. На базе продуктов тяжелого органического синтеза получают СМС, лекарственные препараты, ядохимикаты, пластмассы, волокна.
Как правило, это расчетные задачи по уравнениям химических реакций. При решении таких задач применяются основные законы и формулы для нахождения выхода продукта, массы, количества и т.д.
При решении задач используются как структурные формулы, так и брутто-формулы.
Примеры решения задач
1. При взаимодействии салициловой кислоты с уксусным ангидридом получают ацетилсалициловую кислоту, известную в медицине под названием «аспирин»:
Рассчитайте массу аспирина, который можно получить из 690 кг салициловой кислоты, если массовая доля выхода продукта составляет 75% от теоретически возможного.
Решение:
В уравнении реакции можно написать как структурные формулы, так и брутто-формулы.
С7Н12О3 + С4Н6О3 → С8Н14О4 + СН3СООН
салициловая кислота уксусный ангидрид аспирин уксусная кислот
Находим количество салициловой кислоты.
ν(С7Н12О3)=![]()
По уравнению ν(С7Н12О3)= ν(С8Н14О4)=4792 моль
mтеор(С8Н14О4)=4792 моль*174 г/моль=833808г.
Находим mпр
![]()
Ответ: 625 кг.
Задачи для самостоятельного решения
1. В промышленности винилхлорид получают пиролизом дихлорэтана:
2С2Н4 + 2НС1 → С2Н3С1 + НСl. В настоящее время осуществлен сбалансированный синтез дихлорэтана, при котором получают единственный продукт процесса — винилхлорид. Для этого выделяющийся при пиролизе дихлорэтан смешивают с этиленом и подвергают окислительному хлорированию на катализаторе, содержащем хлорид меди(II) на носителе. Напишите уравнение реакции и рассчитайте объем хлороводорода (н. у.), выделившегося при пиролизе 19,8 кг дихлорэтана, и массу винилхлорида, полученного при сбалансированном синтезе. Какой объем займет этилен (н. у.), необходимый для второй стадии процесса?
2. Полимеризацией хлоропрена получают хлоропреновые каучуки, характеризующиеся высокой устойчивостью к действию света, теплоты и растворителей. Найдите молекулярную формулу хлоропрена, если известно, что массовые доли элементов в нем составляют: углерода — 54,24%, водорода — 5,65%, хлора — 40,11%. Относительная плотность его паров по водороду равна 44,25.
3. Полимеризацией стирола получают полистирол, который используют в электротехнике в производстве декоративно-отделочных материалов и предметов бытового назначения. Найдите молекулярную формулу стирола, если известно, что массовая доля углерода в нем составляет 92,3%, водорода — 7,7%. Относительная молекулярная масса стирола равна 104.
4. Один из многоатомных спиртов используют для приготовления антифризов — жидкостей, замерзающих при низкой температуре. Антифризы используют в зимних условиях для охлаждения автомобильных двигателей. Найдите молекулярную формулу этого спирта, если массовая доля углерода в нем составляет 38,7%, водорода — 9,7%, кислорода — 51,6%. Относительная плотность его паров по водороду равна 31. Напишите структурную формулу спирта и назовите его.
5. Наиболее перспективный способ получения уксусного альдегида — прямое окисление этилена кислородом в присутствии катализаторов — хлоридов палладия и меди. Напишите уравнения реакций и рассчитайте какой объем этилена (н.у.) израсходуется на получение 200 кг уксусного альдегида, если массовая доля выхода его составляет 96% от теоретически возможного?
6. Алкены широко используют для получения альдегидов методом оксосинтеза. Сущность этого метода заключается во взаимодействии алкена с синтез-газом (смесь оксида углерода(II) и водорода) при нагревании и в присутствии специального катализатора. Напишите уравнения реакций. Какой объем этилена (н.у.) расходуется на получение 360 кг пропаналя методом оксосинтеза, если массовая доля выхода альдегида составляет 90% от теоретически возможного?
7. В промышленности муравьиную кислоту получают нагреванием оксида углерода (II) с порошкообразным гидроксидом натрия с последующей обработкой образовавшегося формиата натрия серной кислотой:
+ СО 4Н2SО4
NaОН → НСООNа → НСООН.
- NaHSO4
Какую массу муравьиной кислоты можно получить из 112 кг оксида углерода(II), если массовая доля выхода кислоты составляет 86% от теоретически возможного?
8. Двухосновную адипиновая кислоту НООС-(СН2)4-СООН в больших количествах используют для получения синтетического волокна найлона. В пищевой промышленности она может заменять лимонную и винную кислоты. Сейчас адипиновую кислоту получают окислением циклогексана кислородом. Рассчитайте массу адипиновой кислоты, которую можно получить из 336 кг циклогексана, если массовая доля выхода кислоты составляет 75% от теоретически возможного.
9. Взаимодействием этилового спирта с уксусной кислотой получают этилацетат, используемый в производстве нитроцеллюлозных лаков. Определите массу этилацетата, который образуется при взаимодействии 60 кг 80%-ной уксусной кислоты с 70 кг 96%-ного этанола. Массовая доля выхода этилацетата составляет 90% от теоретически возможного.
10-. Изоамилацетат (грушевая эссенция) используют в пищевой и кондитерской промышленности. Определите массу грушевой эссенции, которую можно получить при взаимодействии 66 кг изоамилового спирта и 112,5 кг 80%-ной уксусной кислоты. Массовая доля выхода эссенции составляет 60% от теоретически возможного.
11. Анилин широко применяют в производстве красителей, фармацевтических препаратов, вспомогательных веществ для резиновой промышленности, полимерных материалов. В последнее время анилин часто получают из хлорбензола и аммиака: С6Н5С1 + 2NH3 → C6H5NH2 + NH4Cl
Определите массу анилина, который можно получить из 450 кг хлорбензола, если массовая доля выхода анилина составляет 94% от теоретически возможного.
12. Поливинилхлорид (ПВХ) используют как упаковочный материал для пищевых продуктов, а также как сырье для производства игрушек, моющих обоев и т.д. Ежегодно в Ханты-Мансийском округе отходы из ПВХ составляет 0,1% от общего количества бытовых отходов – 2 млн. тонн. Напишите уравнения реакций получения ПВХ из метана. Рассчитайте, сколько тонн природного газа (содержание метана 95%) тратится на получение такого количества ПВХ.
3.6 Творческие и изобретательские задачи
В этом разделе не предусматриваются методические рекомендации при решении задач, т.к. диапазон решения теоретических задач очень широк и при решении таких задач происходит акт творчества, находится новый путь в решении сложных проблем или создается нечто новое. Но при решении таких задач студенты опираются на законы химии, физики и математики.
Примеры решения задач
1. а). Чтобы незаметно было, что молоко прокисло, в него добавляли соду. Как это можно выявить?
б) Молоко разбавляли водой, а чтобы прозрачность его не увеличивалась, добавляли крахмал. Как распознать фальсификацию?
Решение:
Вариант 1. В 50 мл кислого молока добавим 10 г пищевой соды, тщательно перемешаем стеклянной палочкой. Ярких внешних изменений нет, но кислый вкус молока исчезает. Происходит реакция нейтрализации молочной кислоты гидрокарбонатом натрия:
CH3-CHOH-COOH + NaHCO3 → CH3-CHOH-COONa + CО2↑+ H2O.
Причем на нейтрализацию молочной кислоты идет только часть гидрокарбоната натрия. Остальная часть гидролизуется:
NaHCO3 + НОН ![]() NaOH + CО2↑ + Н2О;
NaOH + CО2↑ + Н2О;
НСО![]() 3
+ НОН
3
+ НОН ![]() ОН
ОН![]() + СО2↑
+ Н2О.
+ СО2↑
+ Н2О.
Проверив индикаторной бумагой, раствор молока, убеждаемся, что рН равен 9,0. Фенолфталеин меняет окраску в растворе на малиновую, что указывает на щелочную среду. Таким образом, для обнаружения в кислом молоке соды необходимо проверить среду раствора.
Вариант 2. В 32 мл свежего молока добавим 18 мл воды, чтобы раствор не был прозрачным, и 20 г крахмала, тщательно перемешаем. Для обнаружения крахмала в растворе добавим 2-3 капли раствора йода. Цвет молока изменяется на темно-синий. Таким образом, качественная реакция на крахмал вскрывает фальсификацию.
2. Хозяйственное мыло представляет собой смесь натриевых солей нескольких органических кислот с большой молекулярной массой. Если к раствору мыла добавить кислоту, то в результате обменной реакции образуется стеарин, из которого можно изготовить сувенирную свечу. Попытайтесь изготовить свечу из кусочка хозяйственного мыла. При желании сделайте ее окрашенной.
Решение:
Ножом нарезаем кусочки хозяйственного мыла и складываем их в чистую консервную банку. Наливаем воды, чтобы она с избытком накрывала кусочки мыла, и ставим банку на водяную баню, непрерывно помешивая ее содержимое до растворения. Когда мыло полностью растворится и раствор станет однообразной кашицей, консервную банку снимаем с водяной бани и приливаем (осторожно!) 7-8 мл 2 н. раствора уксусной кислоты. Под действием уксусной кислоты из раствора выделяется и всплывает на поверхность густая белая масса - стеарин (смесь стеариновой С17Н35СООН и пальмитиновой С15Н31СООН кислот):
C17H35COONa + CH3COOH →С17Н35СООН + CH3COONa.
стеарат натрия уксусная кислота стеарин ацетат натрия
Даем ей остыть и, собирая стеарин с поверхности ложкой, перекладываем его в чистую посуду. Затем два-три раза промываем водой и заворачиваем в чистую белую тряпку или фильтровальную бумагу, чтобы впиталась лишняя влага. Обезвоженный стеарин расплавляем. Для изготовления свечи окунаем многократно толстую витую нить в полученный расплавленный стеарин, каждый раз давая стеарину затвердеть на фитиле. Поступать, таким образом, следует до тех нор, пока на фитиле не нарастет свеча достаточной толщины.
Чтобы получить красивую фигурную свечу, фитиль желательно сначала пропитать 1-2 слоями стеарина и закрепить в форме так, чтобы он проходил точно по центру формы и был немного натянут. Затем в форму заливают горячий стеарин. Для окрашивания свечи в рабочую смесь вводят ионы
(Сг3+ — зеленый, Си2+ — голубой, Ni3+ — светло-зеленый, Со2+ - синий). Данный опыт можно проводить при изучении темы «Жиры» в X классе, а также на факультативных занятиях.
3. Как вытряхнуть песок из чернильницы-непроливайки? Примерно с такой проблемой столкнулись инженеры-литейщики. Отлитые из металла детали очищают струей песка. Поверхность деталей становится чистой, но отдельные песчинки попадают во внутренние полости и там остаются. Переворачивать тяжелые металлические детали и вытряхивать из них песок невозможно. Что делать?
Решение:
Используем изученный — «использование фазовых переходов».
Сначала надо четко сформулировать противоречие, которое нужно устранить: песок должен быть, чтобы очищать, и песка не должно быть, чтобы не загрязнять полости. Слово «песок» заменяем словом «вещество» - ведь абразивными свойствами обладает не только песок. Противоречие принимает вид: вещество должно быть, чтобы очищать, и вещество должно исчезнуть, чтобы не загрязнять полости. Известно, что вещество просто так исчезнуть не может, оно может только измениться, например, перейти в другое агрегатное состояние при изменении температуры. Подбираем вещество, которое, будучи твердым, выполнит работу, а потом исчезнет. Большинство веществ при повышении температуры сначала переходят в жидкое состояние, а жидкость тоже трудно удалить из полости. Значит, останавливаемся на явлении возгонки (сублимации). Известные учащимся вещества, способные возгоняться, - это йод, белый фосфор, «сухой лед». Для возгонки йода требуется высокая температура, белый фосфор огнеопасен и ядовит. Решение найдено: надо использовать «сухой лед», который после работы испарится, превратившись в газ.
4. Как изготовить конфеты в виде шоколадных бутылочек, наполненных густым малиновым сиропом? Учащиеся чаще всего предлагают сначала сделать шоколадную бутылочку, а потом залить в нее сироп. Однако сироп обязательно должен быть густым, иначе конфета получится непрочной. А густой сироп трудно залить в бутылочку. Можно, конечно, нагреть сироп, он станет более жидким. Но вот беда - горячий сироп расплавит шоколадную бутылочку. Как быть?
Решение:
Используем прием «сделать наоборот», т. е. не сироп заливать в бутылочку, а шоколадом покрывать сироп. Но возникает новое противоречие: как можно покрыть шоколадом жидкий сироп? Опять применяем тот же прием: пусть жидким будет шоколад, а сироп твердым. Придется изменить агрегатное состояние: сироп нужно заморозить в форме бутылочки и окунуть в жидкий шоколад. Шоколад застынет, а сироп растает. Конфетка готова.
Прием «сделать наоборот» — один из самых распространенных в изобретательстве. Закрепить знания о возможностях этого приема можно на примерах нескольких великих открытий: закона Ньютона (ученый задал себе вопрос: почему Земля не падает на яблоко? Попытавшись на него ответить, он сделал открытие). Закона Архимеда (он тоже сделал наоборот: измерил не объем предмета, погруженного в воду, а объем воды, им вытесненной. Это привело к открытию); гелиоцентрического устройства мира (Джордано Бруно предположил, что не Солнце движется вокруг Земли, а Земля вокруг Солнца, и оказался прав, хоть это предположение и стоило ему жизни).
5. Кристаллы оксида алюминия выращивают из очень чистого расплава. Нельзя даже плавить оксид алюминия в платиновом тигле — в расплав могут попасть атомы платины. Как получить сверхчистый расплав?
Решение:
Выявляем и формулируем противоречие: сосуд должен быть, чтобы расплав не разлился, и сосуда не должно быть, чтобы расплав не загрязнялся. Выбираем прием, соответствующий данному противоречию, — это «использование принципа однородности»: объекты, взаимодействующие с данным объектом, должны быть сделаны из того же материала или близкого ему по свойствам. В соответствии с этим принципом придется плавить оксид алюминия в... оксиде алюминия. Любой сосуд, наполненный оксидом алюминия, следует нагревать так, чтобы расплавилась только центральная часть. Получится расплав оксида алюминия в «тигле» из твердого оксида алюминия. Но тут же возникает следующая проблема: как нагреть оксид именно в центре, не прикасаясь к нему? Вспоминая физику, выясняем, что для нагрева без прямого контакта надо использовать электромагнитную индукцию: при этом источник энергии не соприкасается с нагреваемым веществом. Но твердый оксид алюминия — диэлектрик, он не проводит электрический ток. Значит, электромагнитная индукция не может возникнуть. Правда, расплавленный оксид проводит ток, но для плавления нужен нагрев.
Итак, возникает следующее противоречие: в оксид алюминия необходимо добавить кусочки металла, чтобы возникала электромагнитная индукция, и нельзя добавлять кусочки металла, потому что загрязнение оксида недопустимо. Для устранения этого противоречия используем принцип дробления, т. е. разделение объекта на независимые части — алюминий и кислород.
Изобретение оказалось удивительно простым. В оксид алюминия перед началом плавки вводят кусочки алюминия, который хорошо проводит электрический ток и поэтому йод действием электромагнитного поля быстро нагревается сам и нагревает оксид до плавления. Теперь, когда алюминий не нужен (расплавленный оксид сам проводит ток), он исчезает — просто-напросто сгорает при высокой температуре, превращаясь в оксид алюминия.
6. Одна из самых драматических истории в изобретательстве связана с обыкновенной электрической лампой. Неразрешимое, казалось бы, противоречие надолго затормозило развитие этого технического устройства. Чтобы улучшить качество излучения, сделать свет лампы более похожим на солнечный, нужно повысить температуру нити накала. Но чем выше температура нити, тем быстрее идет испарение металла: нить становится тоньше, перегорает, на внутренней поверхности колбы быстро образуется темный налет испарившегося вольфрама, преграждающий путь свету, лампа еще больше разогревается, светимость падает. Как решить задачу?
Решение:
Формулируем противоречие: вольфрамовая нить должна накаляться, но не должна испаряться. В данном противоречии заданы параметры нового вещества для нити накала. Но подобное вещество еще не получено, т. е. избавиться от вредного влияния (испарение вольфрамовой нити) прямым путем мы не можем.
Придется обратить вред в пользу. Уточним, что происходит в лампе.
При высокой температуре амплитуда колебаний атомов вольфрама в кристаллической решетке возрастает настолько, что отдельные атомы отрываются от нити и улетают. Куда? В соответствии с законами физики теплота переносится от более нагретого тела (нити) к менее нагретому (колбе). Как заставить атомы вольфрама вернуться назад и «приземлиться» на старое место, причем не где попало, а именно там, откуда их больше всего вылетает? Физические законы страшнее юридических, их невозможно нарушить даже при очень сильном желании. Перенос вольфрама из холодной зоны в горячую и точная «посадка» на нить накала противоречат законам физики. Здесь поможет химия. Известны так называемые транспортные реакции, при которых твердые или жидкие вещества, взаимодействуя с газообразными, образуют газообразные продукты, а полученные вещества после переноса в другую часть системы при повышении температуры разлагаются с выделением исходного вещества. Такой перенос может происходить как из холодной зоны в горячую, так и в обратном направлении. Параметры заданы. Осталось определить соединение вольфрама, обладающее транспортными функциями. В ртутной лампе используют бром (или хлор). В лампах накаливания в роли «извозчиков» может работать, например, йод. Он взаимодействует с осевшим на колбу вольфрамом, образуя йодид вольфрама(II), который разлагается на раскаленной нити, и вольфрам оседает туда, откуда он испарился. Замечательно то, что этот процесс не потребляет энергию извне, не требует никаких дополнительных обслуживающих систем — все обеспечивается безупречным поведением «дрессированных» молекул.
7. В одном институте разрабатывали проект не совсем обычного трубопровода: по одним и тем же трубам должны были друг за другом идти разные жидкости. Чтобы они не спешивались, их надо разделить специальным устройством, например, после первой жидкости идет шар, словно поршень, а за шаром другая жидкость. Такая система ненадежна, так как при большом давлении в трубопроводе жидкости будут смешиваться. Можно использовать другие разделители, например пробку из трех резиновых дисков. Но любой разделитель не пройдет через насосы, установленные на насосных станциях. Предложите разделитель, способный проходить через насосы и гарантирующий несмешивание жидкостей.
Решение:
Начнем с дробления: мысленно уменьшаем размеры шара. Вместо одного большого шара - множество футбольных мячей. Или теннисных. Или еще меньше - дробинок, плавающих в жидкости. (На такую «пробку» выдано авторское свидетельство.) Замена жесткой пробки на динамичную соответствует общей тенденции развития технических систем. А если продолжить мысленный эксперимент? Перейдем от дроби к еще более мелким частицам - молекулам. Возникает идея пробки из жидкости или газа. Газовая пробка не сможет быть разделителем: транспортируемая жидкость пройдет сквозь нее. А вот жидкая пробка возможна. Один нефтепродукт, например керосин, затем водяная пробка, а за ней другой нефтепродукт, скажем бензин. У жидкой пробки огромные преимущества: она никогда не застрянет в трубопроводе и свободно пройдет через насосы промежуточных станций. Но и недостаток у этой пробки существенный: нефтепродукты будут проникать в жидкий разделитель, головная и хвостовая части пробки постепенно смешаются с ними. Отделить их от воды трудно, на конечной станции пробку и попавшие в нее нефтепродукты придется выбросить. Но жидкое вещество пробки, прибыв в резервуар на конечной станции, должно само отделиться от нефти. Для этого есть только две возможности: жидкость становится твердым веществом и выпадает в осадок или превращается в газ и улетучивается. Переход в газ заманчивее, так как твердый осадок надо отфильтровывать. Значит, нужно вещество, которое при высоком давлении в нефтепроводе (десятки атмосфер) будет жидким, а при нормальном давлении — газообразным. Кроме того, учтем, что подобное растворяется в подобном. Чтобы пробка не растворялась в нефти, ее нужно изготовить из полярной жидкости, дешевой, безопасной, инертной по отношению к нефтепродуктам. Имея столь подробный перечень примет, нетрудно найти подходящее вещество по справочнику. Всеми интересующими нас качествами обладает аммиак. Пробка из жидкого аммиака надежно разделит идущие по трубопроводу жидкости. В дороге она частично смешается с нефтепродуктами, но это нестрашно: на конечной станции аммиак превратится в газ, в нефть останется в резервуаре.
8. Для изготовления листового стекла раскаленную стеклянную ленту подают на конвейер. Лента перекатывается с одного металлического ролика на другой, постепенно остывая. При этом не застывшая еще стеклянная лента прогибается, на стекле образуются неровности, поэтому его приходится долго полировать. Впервые столкнувшись с этой проблемой, инженеры предложили сделать ролики как можно тоньше, чтобы стеклянная лента получалась ровнее. Но чем тоньше ролики, тем сложнее изготовить из них огромный - в десятки метров — конвейер. Если толщина ролика равна толщине спички, на каждый метр конвейера потребуются 500 роликов и устанавливать их придется прямо-таки с ювелирной точностью. Как усовершенствовать процесс изготовления листового стекла?
Решение:
Попробуем опять применить принцип дробления. Уменьшаем диаметр роликов. Минимальная толщина — один атом. Раскаленная стеклянная лента движется по слою шариков-атомов. Отличный конвейер, идеально ровный.
Итак, под стеклянную ленту надо насыпать шарики-атомы. Это не могут быть атомы газа (они сразу улетучатся) или твердого тела (они не будут свободно двигаться). Остается одна возможность — использовать атомы жидкости. Какую жидкость взять для такого конвейера? Не будем искать наугад, используем знания по химии (или хотя бы справочники). Прежде всего, нужна жидкость легкоплавкая, но у нее должна быть высокая температура кипения, иначе она легко закипит, и поверхность стекла покроется пузырьками. Плотность жидкости должна значительно превышать плотность стекла (2,5 г/см3), иначе стеклянная лента не будет держаться на ее поверхности. Итак, искомое вещество имеет температуру плавления не выше 200-300°С, температуру кипения не ниже 1500 °С, плотность не менее 5-6 г/см3.
Таким сочетанием свойств обладают только металлы. Если не брать во внимание редкие металлы, претендентов совсем мало: висмут, олово, свинец. Висмут дорог, пары свинца ядовиты, остается олово. Итак, вместо конвейера — длинная ванна с расплавленным оловом. Вместо роликов — атомы.
Система перешла на микроуровень, появилась возможность дальнейшего развития. И действительно, сразу после этого изобретения потоком пошли патенты на различные усовершенствования. Например, если через олово пропустить ток, то с помощью магнитов можно придавать его поверхности любую форму - только на эту тему сделано несколько сотен изобретений.
9. При выплавке чугуна в домне образуется ишак. Шлак, имеющий температуру 1000°С, спивают в большие ковши и на железнодорожных платформах отвозят на переработку. Расплав шлака — ценное сырье для изготовления строительных материалов. Но затвердевший шлак перестает быть таким сырьем. Снова расплавлять его невыгодно. В ковше сначала весь шлак жидкий, однако при транспортировке на его поверхности образуется и быстро нарастает твердая корка. Приходится пробивать ее с помощью специальных (довольно громоздких) устройств. Корка удерживает часть жидкого шлака. В результате из ковша сливают только 2/3 шлака, остальное идет на свалку. К тому же нужно потратить немало труда, чтобы освободить ковш от затвердевшего шлака, а потом вывезти этот шлак с территории завода. Было бы выгодно сделать ковш с хорошей теплоизоляцией, но она займет много места, ковш станет шире, а это недопустимо при железнодорожных перевозках. Если же сделать теплоизолирующую крышку на ковш, который размером с комнату, то и устанавливать, и снимать ее придется с помощью крана. Предложите решение.
Решение:
Модель задачи: есть раскаленный шлак, а над ним холодный воздух. ИКР: холодный воздух сам не дает застыть шлаку. Применяем прием «обратить вред в пользу»: холодный воздух должен защищать шлак от холодного воздуха.
Какая зона воздуха не соответствует этому требованию? Очевидно, та, которая непосредственно соприкасается с горячей поверхностью расплавленного шлака. Теперь видно физическое противоречие: эта зона (там сейчас слой холодного воздуха) должна быть чем-то заполнена, чтобы задерживать тепло, и эта зона не должна быть ничем заполнена, чтобы можно было свободно заливать и выливать шлак. В подобных случаях не вводят посторонние вещества, а видоизменяют уже присутствующие («использовать принцип однородности») – шлак и воздух. Возможны только три ответа.
Изменять воздух – нагревать тот слой, который лежит у поверхности шлака. Это плохое решение: придется ставить горелки, а они будут загрязнять атмосферу.
Изменять шлак – покрыть поверхность жидкого шлака шариками из твердого шлака. Термоизоляция получится неплохая, но возникает масса неудобств: надо изготавливать шарики, как-то удерживать их в ковше, когда сливается шлак.
Использовать смесь шлака и воздуха – смешать компоненты и получить пену. Отличный теплоизолятор. Залили шлак в ковш, сделали слой пены, получили прекрасную теплозащитную крышку. Сливать шлак можно, не обращая внимания на эту крышку, - жидкий шлак свободно пройдет сквозь пену. Крышка есть, и как бы нет. Задача в принципе решена, нужно выяснить чисто технический вопрос: как получить пену? Простейший способ – при заливке шлака подавать одновременно немного воды. Обратите внимание на парадокс: чтобы шлак сохранил тепло его поливают холодной водой.
10. Хороший термос долго (до 2 суток) хранит тепло, но когда жидкость в термосе остыла, то для нагревания ее необходимо вылить из термоса, нагреть и снова залить. А если для этого нет условий? Почему бы воду не нагреть сразу в термосе? Но колба термоса не герметична, в простенках вакуум. Если в колбу ставить еще один металлический цилиндр, чтобы в нем нагревать воду, вес изделия увеличится. Это грубое решение проблемы. Изобретите термос – чайник.
Решение:
Формулируем техническое противоречие: вакуум в колбе должен быть теплопроводным, когда вода нагревается, и не должен проводить тепло, когда нагревание прекращено. Заменяем слово вакуум на словом вещество: вещество в сосуде должно проводить тепло при нагревании сосуда и быть теплоизолятором при прекращении нагревания. Лучший теплоизолятор тепла – вакуум. Уточняем: вещество появляется при нагревании и проводит тепло; вещество исчезает при прекращении нагревания, образуется вакуум. Для решения этой задачи более всего подходят гидриды металлов, т.к. они обладают способностью поглощать водород при охлаждении и выделять при нагревании. А водород хороший проводник тепла. Итак, в термосе между стенками глубокий вакуум, а на дне - горсть гидрида. Если немного нагреть гидрид, то выделившийся водород станет проводником тепла между стенками. Выключим нагрев, и водород полностью поглотится гидридом, восстановится вакуум. Внутри термоса может быть аккумулятор тепла и холода. По энергоемкости водородные термосы в 20 раз превосходят электробатареи.
Выводы
1. Определена тематика задач по теоретическим основам химической технологии в рамках изучения курса прикладная химия.
2. Составлены и подобраны задачи по выбранным темам.
3. Показано, что при решении задач по прикладной химии студенты испытывают затруднения при математических расчетах с использованием дифференциального и интегрального исчисления, разложением сложного многостадийного процесса в условии задачи на отдельные стадии и проведении расчетов по всей совокупности стадий.
4. Разработана методика решения задач, в качестве примера представлены подробные решения типовых задач каждого раздела и приведены задачи для самостоятельного решения.
5. Показано, что курс прикладная химия, изучаемый на завершающем этапе подготовки будущих учителей химии следует рассматривать как курс обобщения, повторения и систематизации ранее приобретенных химических знаний.
Список литературы
1. Абкин Г.Л. Методика решения задач по химии. М.: Просвещение, 1971. – 200 с.
2. Аликберова Л.Ю., Хабарова Е.И. Задачи по химии с экологическим содержанием. М.: Центрхимпресс, 2001. – 70 с.
3. Андреева М.П. Овладение студентами педагогических ВУЗов методическими приемами обучения учащихся решению задач по химии. // Химия и методика преподавания. 2005, № 3. – С. 23-26.
4. Аранская О.С. Сборник задач и упражнений по химической технологии и биотехнологии. Минск: Университетское, 1989. – 296с
5. Аркавенко Л.Н., Гапонцеа В.Л., Белоусова О.А. Для чего классифицировать расчетные задачи. // Химия в школе. 1998, № 3. – С. 60-63.
6. Артемьев В.П. Задание по методике преподавание химии. Тесты и усложненные задачи (задачи экологического содержания). Пенза, 2002. 122 с.
7. Архангельская О.В., Тюльков И.А. Трудная задача? Начнем по порядку…
// Химия в школе. 2003, № 2. – С. 51-55.
8. Ахметов М.А. Конспект лекции по общей химии. Введение в термодинамику химических реакций. // Первое сентября. 2005, № 15. – С. 35-37.
9. Безуевская В.А. Химические задачи с экологическим содержанием. // Химия в школе. 2000, №2. – С. 59-61.
10. Бердоносов С.С. Конспект лекции по общей химии. Тепловые эффекты химических реакций. // Первое сентября. 2005, №20 – С. 11-18.
11. Бердоносов С.С. Конспект лекции по общей химии. Равновесие. // Первое сентября. 2005, №21. – С. 18-23.
12. Бондарь Д.А., Гариев И.А. Трудная задача? Начнем по порядку… // Химия в школе. 1997, № 3. – С. 44-48.
13. Бондарь Д.А., Тюльков И.А. Трудная задача? Начнем по порядку. // Химия в школе. 1999, №2. – С. 31-34.
14. Бондарь Д.А., Гариев И.А. Трудная задача? Начнем по порядку… // Химия в школе. 1997, № 6. – С. 61-64.
15. Веденяпин А.В. Решение расчетных задач по химии. М.: Просвещение, 1972. – 160 с.
16. Гаврусейко Н.П. Наш опыт решения расчетных задач. // Химия в школе. 1981, № 1. – С. 46-50.
17. Гольдфарб Я.Л., Ходаков Ю.В., Додонов Ю.Б. Сборник задач и упражнений по химии. М.: Просвещение, 1988. – 156 с.
18. Гудкова А.С., Ефремова К.М., Магдесиева Н.Н., Мельчакова Н.В. 500 задач по химии. М.: Просвещение, 1977. – 120 с.
19. Гузеев В.В. О системе задач и задачном подходе к обучению. // Химия в школе. 2001, № 8. – С. 12-14.
20. Ерыгин Д.П., Шишкин Е.А. Методика решения задач по химии. М.: Просвещение, 1989. – 176 с.
21. Ерыгин Д.П. Фоминых Н.А. Задачи экологического содержания в курсе органической химии. // Химия в школе. 1992, №5-6. – С. 47-49.
22. Задачи и упражнения по общей химии. Под редакцией профессора Н.В. Коровина. М.: «Высшая школа», 2006. – 155 с.
23. Зуева М.В. Развитие учащихся при обучении химии. М.: Просвещение, 1978. – 184 с.
24. Игнатенков В.И., Бесков В.С. Примеры и задачи по общей химической технологии. М.: ИКЦ «Академкнига», 2005. – 200 с.
25. Керимов Э.Ю. Курс лекций по физической химии: химическая термодинамика. Пенза, 2005. – 104 с.
26. Керимов Э.Ю. Курс лекций по физической химии: химическая кинетика. Пенза, 2004. – 109 с.
27. Кирюшкин Д.М. Методика обучения химии: Просвещение, 1970. 186 с.
28. Климов И.И., Филько А.И. Сборник вопросов и задач по физической и коллоидной химии. М.: Просвещение, 1975. – 190 с.
29. Ключников Н.Г. Практические занятия по химической технологии. М.: Просвещение, 1972. – 165 с.
30. Кудряшов И.В., Каретников Г.С. Сборник примеров и задач по физической химии. М.: Высшая школа, 1991. – 510 с.
31. Кушнарев А.А. Учимся решать задачи по химии. // Химия в школе. 1993,
№ 5. – С. 46-54.
32. Кушнарев А.А. Учимся решать задачи по химии. // Химия в школе. 1994,
№ 2. – С. 44-51.
33. Кушнарев А.А. Учимся решать задачи по химии. // Химия в школе. 1995, № 5. – С. 51-57.
34. Лабий Ю.Н. Решение задач по химии с помощью уравнений и неравенств. М.: Просвещение, 1987. – 80 с.
35. Логинов Н.Я., Ключков Н.Г. Практикум по химической технологии. М.: Просвещение, 1963. – 210 с.
36. Магдесиева Н.Н., Кузменко Н.Е. Учись решать задачи по химии. М.: Просвещение, 1986. – 259 с.
37. Мациевский А.Э. К методике решения задач на тепловые эффекты. // Химия в школе. 1979 № 4. – С. 54-57.
38. Методика преподавания химии. Под редакцией Кузнецовой Н.Е. М.: Просвещение, 1984. – 406 с.
39. Мурзина Т.Б, Оржековский П.А. Новые подходы в обучении решению расчетных задач по химии. // Химия и методика преподавания. 2002, № 8. – С. 28-33.
40. Пичугина Г.В. Задание для самостоятельной работы по курсу прикладной химии. // Химия в школе. 1997, № 3. – С. 29-31.
41. Плетнер Ю.В., Полосин В.С. Практикум по методике преподавания химии. М.: Просвещение, 1981. – 210 с.
42. Протасов П.Н., Цитович И.К. Методика решения расчетных задач по химии. М.: Просвещение, 1978. – 123 с.
43. Радецкий А.М. Задачи с производственным содержанием по органической химии. // Химия в школе. 1996, № 1. – С. 40-41.
44. Соколов Р.С. Химическая технология том 1. М.: ВЛАДОС, 2003. – 363 с.
45. Соколов Р.С. Химическая технология том 2. М.: ВЛАДОС, 2003. – 444 с.
46. Строкатов С.Ф., Майзель В.В., Ильинова Г.Н., Юркъян О.В. Методика решения расчетных химических задач. // Химия в школе. 1999, № 5. С. 60-61.
47. Стромберг А.Г., Семченко Д.П. Физическая химия. М.: Высшая школа, 2001. – 516 с.
48. Тюльков И.А. Трудная задача? Начнем по порядку… // Химия в школе. 2000, № 3. – С. 56-60.
49. Хомченко Г.П. Пособие по химии для поступающих в ВУЗы. М.: Новая волна, 1997. – 447 с.
50. Хомченко Г.П., Хомченко И.Г. Сборник задач по химии для поступающих в ВУЗы. М.: Новая волна, 2001. – 271 с.
51. Цитович И.К., Протасов П.Н. Методика решения расчетных задач по химии. М.: Просвещение, 1983. – 245 с.
52. Чернобельская Г.М. Методика обучения химии в средней школе. М.: ВЛАДОС, 2000. – 303 с.
53. Чечевицына М.Б. Использование теории решения изобретательских задач // Химия в школе. 2004, № 4. – С. 26-38.
54. Чунихина Л.Л. Из опыта обучения решению расчетных задач // Химия в школе. 1900, № 3. – С. 33-36.
55. Шаповаленко С.Г. Методика обучения химии, М.: Просвещение, 1963. – 660 с.
56. Шишкин Е.А. Пути решения расчетной задачи. // Химия в школе. 2005, № 4. – С. 46-52.
57. Штремплер Г.И Хохлова А.И. Методика решения расчетных задач по химии. М.: Просвещение, 1998. – 195 с.