
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
Психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Реферат: Лантаноиды и актиноиды
Реферат: Лантаноиды и актиноиды
1. Строение.
Лантаноиды и актиноиды располагаются в третьей побочной группе Периодической системы. Эти элементы следуют в таблице сразу после лантана и актиния и поэтому их называют соответственно лантаноиды и актиноиды. В короткой форме Периодической системы Д.И. Менделеева они вынесены в два последних ряда. Они относятся к f-элементам.
У в атомах лантаноидов и актиноидов происходит заполнение соответственно 4f- и 5f-подуровней.
Лантаноиды очень сходны по химическим свойствам. Близость свойств соединений лантаноидов обусловлена тем, что застройка внутренней 4f-оболочки атомов мало сказывается на состоянии валентных электронов. В образовании химической связи 4f-электроны лантаноидов обычно не принимают участия.
Электроны заполняют 4f-, а не 5d-подуровень потому, что в этом случае они обладают меньшей энергией. Однако разница в энергиях 4f- и 5d-состояний очень мала. Благодаря этому один из 4f -электронов (а в некоторых случаях, например, у церия, два 4f--электрона) легко возбуждается, переходя на 5d-подуровень, и становится, таким образом, валентным электроном. Поэтому в большинстве своих соединений лантаноиды имеют степень окисления +3, а не +2. Это обстоятельство объясняет близость свойств лантаноидов к свойствам элементов подгруппы скандия.
В пределах одного периода с возрастанием порядкового номера размеры атомов элементов уменьшаются. Подобная закономерность наблюдается не только для элементов главных подгрупп, но, за немногими исключениями, и для элементов побочных подгрупп. Такое же уменьшение радиусов атомов имеет место и в случае лантаноидов (лантаноидное сжатие).
Как и в случае лантаноидов, у элементов семейства актиноидов происходит заполнение третьего снаружи электронного слоя (подуровня 5f); строение же наружного и, как правило, предшествующего электронных слоев остается неизменным. Это служит причиной близости химических свойств актиноидов. Однако различие в энергетическом состоянии электронов, занимающих 5f- и 6d-подуровни в атомах актиноидов, еще меньше, чем соответствующая разность энергий в атомах лантаноидов. Поэтому у первых членов семейства актиноидов 5f-электроны легко переходят на подуровень 6d и могут принимать участие в образовании химических связей. В результате от тория до урана наиболее характерная степень окисления элементов возрастает от +4 до +6. При дальнейшем продвижении по ряду актиноидов происходит энергетическая стабилизация 5f-состоянии, а возбуждение электронов на 6d-подуровень требует большей затраты энергии. Вследствие этого от урана до кюрия наиболее характерная степень окисления элементов понижается от +6 до +3 (хотя для нептуния и плутония получены соединения со степенью окисления этих элементов +6 и +7). Берклий и следующие за ним элементы во всех своих соединениях находятся в степени окисления +3.
2. Свойства.
Ø Свойства лантаноидов.
В виде простых веществ все лантаноиды представляют собой серебристо - белые металлы (желтизна празеодима и неодима обусловлена образованием на поверхности пленки оксидов). Они хорошо куются. Почти все лантаноиды парамагнитны, только гадолиний, диспрозий и гольмий проявляют ферромагнитные свойства.
В ряду Се—Lu в изменении плотности, температур плавления и кипения проявляется внутренняя периодичность, т. е. указанные свойства металлов подсемейства церия изменяются с такой же последовательностью, как и у металлов подсемейства тербия (табл.1 ).
Таблица 1.
Физические свойства лантаноидов
| Металл |
Плотность, кг/м3 |
Температура , 0 С |
|
| плавления | кипения | ||
|
Подсемейство церия |
|||
| Лантан | 6120 | 920 | 3420 |
| Церий | 6770 | 804 | 3470 |
| Празеодим | 6770 | 935 | 3017 |
| Неодим | 7010 | 1024 | 3210 |
| Прометии |
— |
— |
— |
| Самарий | 7540 | 1072 | 1670 |
| Европий | 5240 | 826 | 1430 |
| Гадолиний | 7890 | 1312 | 2830 |
|
Подсемсйстео тербия |
|||
| Тербий | 8250 | 1368 | 2480 |
| Диспрозий | 8560 | 1380 | 2330 |
| Гольмий | 8780 | 1500 | 2380 |
| Эрбий | 9060 | 1525 | 2390 |
| Тулий | 9320 | 1600 | 1720 |
| Иттербий | 6950 | 824 | 1320 |
| Лютеций | 9850 | 1675 | 2680 |
Температуры плавления в этом ряду возрастают, исключение составляют только европий и иттербий. Они имеют также относительно более низкие, чем у остальных элементов, температуры кипения.
Лантаноиды, как и лантан, по реакционной способности уступают лишь щелочным и щелочноземельным металлам. Во влажном воздухе они быстро тускнеют (вследствие образования оксида) , а при нагревании до 200—400°С на воздухе воспламеняются и сгорают с образованием смеси оксидов (Э203) с нитридами (ЭN). Церий в порошкообразном состоянии даже при обычных условиях легко воспламеняется на воздухе. Это свойство церия нашло применение при изготовлении кремней для зажигалок.
4Э +3О2 =2Э2О3
Лантаноиды взаимодействуют с галогенами, а при нагревании — с азотом, серой, углеродом, кремнием, фосфором, водородом.
2Э +3Cl2=2ЭCl3
2Э +N2= 2ЭN
Э +2S = ЭS2
Э + 2 С = ЭС2 или 2Э + 3С = Э2С3
Э + Н2 = ЭН2
Карбиды, нитриды и гидриды лантаноидов взаимодействуют с водой с образованием гидроксида и соответственно ацетилена или различных углеводородов, аммиака и водорода.
ЭN + 3Н2О = Э(ОН)3 +NН3
ЭС2 + Н2О = Э(ОН)3 +С2Н2
ЭН2 +Н2О = Э(ОН)3 +Н2
Находясь в ряду напряжений значительно левее водорода (электродные потенциалы их колеблются е пределах от —2,4 до —2,1 В), лантаноиды окисляются горячен водой по реакции:
2Э + 6Н20 = 2Э(ОН)3 + 3Н2.
Они хорошо взаимодействуют с разбавленными растворами НС1, HN03 и H2S04.
2 Э +6НCl =2 ЭСl3 +3H2
В растворах фосфорной и плавиковой кислот лантаноиды устойчивы, так как образуют защитные пленки малорастворимых солей. В водных растворах щелочей лантаноиды не растворяются. Химическая активность элементов в ряду Се—Lu несколько снижается, что связано с уменьшением радиусов их атомов и ионов.
Оксиды лантаноидов отличаются высокой химической прочностью и тугоплавкостью. Например, La203 плавится при температуре выше 2000°С, а Се02 — около 2500°С. В воде они практически нерастворимы, хотя интенсивно (с выделением теплоты) взаимодействуют с ней с образованием соответствующих гидроксидов Э(ОН)3. Гидроксиды также труднорастворимы в воде. В ряду лантаноидов основная сила гидроксидов постепенно уменьшается с уменьшением радиусов в результате лантаноидного сжатия. С уменьшением ионных радиусов увеличивается прочность связи с кислородом. Поэтому гидроксиды последних лантаноидов - иттербия и лютеция – проявляют слабую амфотерность .
Оксиды и гидроксиды лантаноидов растворяются в кислотах (кроме HF и Н3Р04).
Соли лантаноидов со степенью окисления +3 почти не гидролизуются, поскольку Э(ОН)3 -довольно сильные основания. Хорошо растворимые соли (хлориды, нитраты, сульфаты) образуют различные кристаллогидраты. Мало растворимы фториды, карбонаты, фосфаты, оксалаты. Многие соли Э3+ образуют с аналогичными солями щелочных металлов хорошо кристаллизующиеся двойные соли. Раньше их применяли для разделения РЗЭ кристаллизацией.
Э2(SO4)3 + Ме2SO4 = Ме2SO4· Э2(SO4)3
Ионы Э3+ в водном растворе образуют гидратные комплексы [Э(H20)n]3+, n=8. Гидратированные ионы окрашены: Се3+- бесцветный, Рr+3 - желто-зеленый, Nd3+ - красно-фиолетовый, Рm3+ - розовый, Sm3+ -желтый, Eu3+, Gd3+, Tb3+ - бесцветные, Dy3+ - бледно-желто-зеленый, Но+3- коричневато-желтый, Ег+3- розовый, Тm - бледно-зеленый, Yb3+, Lu3+ — бесцветные. Ион Ce4+(p) имеет ярко-желтую окраску.
Некоторые лантаноиды имеют, помимо характеристической, еще степени окисления +4 и +2. Среди лантаноидов, проявляющих степень окисления +4, выделяется церий. Относительно более стабильные соединения в степени окисления +2 дает европий.
Диоксид СеО2 образуется при непосредственном взаимодействии компонентов . Он плавится при 2600 0 С под давлением кислорода, начинает отщеплять кислород только при 2300 0С. При 1250 0С Се02 восстанавливается водородом до Се203. Диоксид церия не растворяется в воде, а после прокаливания и в кислотах, и в щелочах. СеО2 -.является сильным окислителем, например, выделяет хлор из соляной кислоты:
2CeO2 +8HCI = 2CeCl3 +CL2 + H20
Гидроксид церия Се(ОН)4 при взаимодействии с кислотами-восстановителями образует соли со степенью окисления церия +3:
2Се(ОН)4 + 8НС1 = 2СеС13 + С12 + ЗН20.
Из солей кислородсодержащих кислот, содержащих ионы лантаноидов со степенью окисления +4, известны только производные церия. Сульфат Ce(S04)2 получается нагреванием Се02 с горячей концентрированной серной кислотой. Ce(S04)2 — порошок желтого цвета, хорошо растворяется в воде, подвергается гидролизу. Сульфат церия из водных растворов выделяется в виде розовых кристаллов с различным содержанием воды, среди которых доминируют кристаллогидраты с 8 молекулами воды. Известны только основные нитраты и карбонаты: Ce(OH)(N03)3 и Се2(ОН)2(СО3)3. В то же время Се (+4) образует устойчивые ацетат и перхлорат: Се(СН3СОО)4, Се(С104)4.
Для Ce(+4) известны довольно устойчивые комплексы [Се(С2О4)3]'2_ и [Се(N03)6]-2. Из галогенидных комплексов наиболее устойчивы фторидные.
Степень окисления +2 наиболее характерна для европия, хотя известны оксиды, галогениды и сульфаты самария и иттербий в степени окисления +2. Нагреванием на воздухе Eu203 с графитом до 1700 0С получен темно-коричневый оксид ЕuО. Монооксид европия — тугоплавкие кубические кристаллы — медленно разлагается водой с выделением водорода, т. е. является сильным восстановителем. Известны также монооксиды самария и иттербия . Восстановлением EuF3 водородом при 1000 0С можно получить дифторид EuF2. Известны дихлориды, дибромиды, дииодиды Sm, Eu, Tm и Yb. Их устойчивость в указанном ряду лантаноидов снижается слева направо и, естественно, от хлоридов к иодпдам.
Катодным восстановлением сульфатов Э(+3) получены белый EuSO4, светло-зеленый YbSO4, и красный SmSO4.
Все производные лантаноидов в степени окисления +2 являются восстановителями, например :
2 YbSO4 +H2SO4 = Yb2(SO4)3 + H2
Ø Свойства актиноидов
Из актиноидов наибольшее значение имеют лишь торий, уран и плутоний. Поэтому рассмотрим их более подробно.
Торий, уран и плутоний - серебристо-белые твердые металлы, на воздухе быстро покрываются темной пленкой из оксидов и нитридов. Некоторые физические свойства некоторых актиноидов указаны в табл. 2
Таблица 2.
Физические свойства некоторых актиноидов
| Металл |
Плотность, кг/м3 |
Температура, °С | |
| плавления | кипения | ||
| Актиний | - | 1 100 |
- |
| Торий | 11720 | 1750 | 3 000-4 400 |
| Протактиний | 15 370 | 1 873 |
— |
| Уран | 19 040 | 1 132 | 3818 |
| Нептуний | 20 450 | 637 |
— |
| Плутоний | 19 740 | 640 | 3 235 |
| Америций | 13 670 | 995 | 2 607 |
| Кюрий | 13 500 | 1340 | - |
Данные элементы радиоактивны, периоды полураспада для 232Th, 238U и 239Pu составляют соответственно 1,40 •1010, 4,5•109 и 24 400 лет.
Строение внешних электронных оболочек атомов: 6d27s2 , U 5f 36d17s2, Pu 5f6 7s2. Таким образом, в атоме Pu происходит «провал» электрона на 5f-оболочку.
Торий, являющийся аналогом церия, проявляет степени окисления +2, +3 и +4, две первые редки, последняя - характерна. Стабильность степени окисления +4 связана с тем, что ион Th4+ имеет электронную конфигурацию атома Rn. Как уже указано выше, характерными степенями окисления урана являются +4 и +6, последняя представлена большим числом соединений (ион U6+ имеет электронную конфигурацию Rn). Плутоний проявляет степени окисления от +3 до +7, наиболее распространены соединения Pu+4 .
Для остальных актиноидов характерны следующие степени окисления :
протоактиний +4, +5 и +6
нептуний и плутоний наиболее характерна степень окисления +3 и
+4, получены соединения со степенями
окисления+6 и +7
америций и кюрий наиболее характерна степень окисления +3,
имеются соединения со степенью окисления
+4.
берклий следующие наиболее характерна степень окисления +3.
за ним элементы
Актиноиды, подобно лантаноидам, характеризуются высокой химической активностью. В высокодисперсном состоянии Th, U и Pu активно поглощают водород, образуя нестехиометрические металлоподобные соединения, состав которых приближается к ЭНз. Термическое разложение UH3 можно использовать для получения особо чистого водорода.
При нагревании в присутствии кислорода эти металлы образуют' оксиды: бесцветный ТhO2, темно-коричневый UO2, желто-коричневый РuO2.
Э +О2 =ЭО2
Это тугоплавкие соединения, особенно ТhO2 (т. пл. 3220 °С). При более сильном нагревании (до красного каления) уран образует темно-зеленый оксид U3O8, формулу этого соединения можно записать U2+4U+6O8 .
Гидроксиды Э(ОН)3 малорастворимы в воде и имеют основный характер. Гидроксиды Э(ОН)4 имеют основный характер и также нерастворимы в воде
Рассматриваемые металлы реагируют с кислотами, образуя соли Э+4.
Э + 2Н2SO4 = Э(SO4)2 + 2H2
Соли, в которых актиноиды находятся в состоянии окисления +4, напоминают по свойствам соли Се4+. Соли актиноидных металлов, в которых последние находятся в степени окисления +3, сходны по свойствам с аналогичными солями лантаноидов.
При действии на уран избытка фтора образуется гексафторид UF6 бесцветное, легко возгоняющееся кристаллическое вещество (давление его пара 101 кПа при 56,5 °С). Это единственное соединение урана, существующее в газообразном состоянии при низкой температуре. Данное обстоятельство имеет большое практическое значение, поскольку разделение изотопов 235U и 238U (с целью получения атомной энергии) осуществляют с помощью процессов, протекающих в газовой фазе (центрифугирование, газовая диффузия). При растворении в воде UF6 гидролизуется
UF6 +2Н2О = UО2F2 +4HF
Тетрафторид UF4 получают действием HF на UО2.
UО2 + 4 HF = UF4 + 2Н2О
Аналогичными свойствами обладают гексафториды нептуния и плутония.
С хлором уран образует легко растворяющийся в воде тетрахлорид UCl4. При избытке хлора получается UCI5, легко диспропорционирующий на UCl4 и UC16 .
При нагревании уран активно взаимодействует с азотом, серой и другими элементными веществами.
Соединения U+4 в подкисленных водных растворах легко окисляются до шестивалентного состояния с образованием ярко-желтых солей уранила. Поскольку с увеличением заряда иона актиноида усиливается его взаимодействие с водой (гидролиз), то в водном растворе ионы Э5+ и Э6+ не существуют. В воде они превращаются соответственно в ионы ЭО2+ и ЭО22+. Связи атомов кислорода с ионами актиноидов в состоянии окисления +5 и +6 настолько прочны, что ионы ЭО2+ и ЭО22+остаются неизменными при многих химических превращениях. Гидроксид уранила при нагревании разлагается, образуя оксид UО3. При действии Н2О2 на раствор нитрата уранила образуется желтый пероксид урана:
U02(N03)2 + Н202 + 2Н20 = U04 •2Н20 ¯ + 2HN03
Для соединений актиноидов чрезвычайно характерны реакции диспропорционирования. Например, ион пятивалентного плутония РuО2+ в водном растворе диспропорционирует на ионы трехвалентного и шестивалентного плутония:
3Pu02+ + 4Н+ = Рu3+ + 2PuO22+ + 2Н20
Многие соли актиноидов хорошо растворимы в различных органических растворителях, не смешивающихся с водой. На этом основана экстракция соединений актиноидов органическими веществами из водных растворов. Экстракционные процессы нашли широкое применение в технологии выделения и разделения, близких по свойствам актиноидов.
3. f –элементы в природе и их применение.
В природе лантаноиды очень рассеяны и в свободном виде не встречаются, а лишь в; сочетании друг с другом или с лантаном и иттрием. При отделении рассматриваемых элементов друг от друга большие трудности возникают ввиду чрезвычайного сходства свойств лантаноидов. Содержание лантана и лантаноидов в земной коре составляет 0,01 %' (масс), т. е. примерно такое же, как меди. Наиболее распространены гадолиний, церий и неодим, наиболее редко гольмий, тулий и лютеций.
Очень редко встречается радиоактивный элемент прометий. Впервые он выделен в 1947 г. из продуктов деления урана в ядерном реакторе.
Лантаноиды обычно получают электролизом расплавленных хлоридов или фторидов. Они могут быть также получены металлотермическим способом при восстановлении фторидов или хлоридов активными металлами.
Лантаноиды используют в производстве особых марок чугуна и высококачественных сталей. Введение, этих элементов в чугун в виде ферроцерия (сплав церия с железом) или сплава различных лантаноидов повышает прочность чугуна. Небольшие добавки лантаноидов к стали очищают ее от серы, азота и других примесей, так как лантаноиды, являясь химически активными металлами, взаимодействуют с примесями. При этом повышаются прочность, жаропрочность и коррозионная устойчивость сталей. Такие стали пригодны для изготовления деталей сверхзвуковых самолетов, оболочек искусственных спутников Земли. С помощью лантаноидов получают также жаропрочные сплавы легких металлов —магния и алюминия. Благодаря сплавам лантаноидов проводят металлотермическое восстановление многих металлов (титана, ванадия, циркония, ниобия, тантала и др.), используя в этом процессе большое сродство лантаноидов к кислороду.
Важную роль играют лантаноиды и в силикатной промышленности. При добавлении к жидкой массе стекла оксидов лантаноидов стекло приобретает высокую прозрачность. Оно становится при этом устойчивым не только к действию ультрафиолетовых лучей, но и к рентгеновскому излучению. Стекла с добавкой лантаноидов необходимы для астрономических и спектроскопических приборов. Стекла окрашиваются в ярко-красный цвет от присутствия Nd203, в зеленый — от Рr203. Оксиды лантаноидов пригодны также для окраски фарфора, глазурей и эмалей.
Оксиды гадолиния, самария и европия входят в состав защитных керамических покрытий от тепловых нейтронов в ядерных реакторах. Соединения лантаноидов входят в состав красок, лаков, люминофоров (светящиеся составы), катализаторов.
Все актиноиды радиоактивны. За период существования Земли большинство из них полностью распалось и в настоящее время в природе не встречаются. Поэтому их получают искусственно. Существование в природе тория, протактиния и урана объясняется тем, что они имеют сравнительно стабильные изотопы, т.е. изотопы с большим периодом полураспада.
Промышленным источником тория служат монацитовые пески. Они также являются сырьем для получения редкоземельных элементов. Известны богатые по содержанию минералы торит ThSi04 и торианит (Th,U)02. Однако они редко встречаются в природе и не образуют больших скоплений.
Протактиний чрезвычайно рассеянный элемент. Его добывают из отходов переработки урана. Однако в настоящее время изотоп протактиния-231 синтезируют искусственным путем в ядерных реакторах. Таким способом его получают в больших количествах, чем из уранового сырья.
Для урана известно около 200 минералов. Однако промышленное значение имеют лишь немногие. К их числу относится минерал настуран (урановая смолка, или урановая обманка). Обычно ему приписывают формулу U3O8. Довольно широко распространен также минерал отэнтит - Ca(U02)2(P04)2•H20. В ничтожных количествах в природе также встречаются нептуний и плутоний. Однако их существование объясняется тем, что в природе происходят ядерные процессы, подобные тем, которые человек производит в ядерных реакторах.
В настоящее время в различных странах мира существует хорошо налаженное производство актиноидных металлов в следующих масштабах (за один год):
Нептуний Десятки килограм- Калифор- Доли грамма
мов ний
Плутоний Тонны Эйнштей- Доли миллиграмма
Америций Десятки килограм- ний
мов Фермий Миллиарды атомов
Кюрий Килограммы Менделевий Тысячи атомов
Берклий Дециграммы
 Из
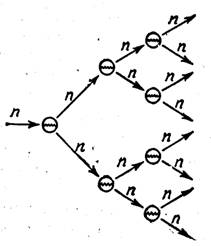
актиноидов наибольшее применение нашли уран и плутоний. Дело в том, что ядра
двух изотопов урана (235U и 233U), а также двух изотопов плутония (239Рu и 241Рu) при
захвате нейтрона способны делиться на два осколка, причем в каждом акте ядерного
деления, наряду с осколками, делящееся ядро испускает два или три нейтрона.
Благодаря этому становится возможным не только продолжение начавшегося деления
ядер, но и лавинообразное его нарастание (рис. 1).
Из
актиноидов наибольшее применение нашли уран и плутоний. Дело в том, что ядра
двух изотопов урана (235U и 233U), а также двух изотопов плутония (239Рu и 241Рu) при
захвате нейтрона способны делиться на два осколка, причем в каждом акте ядерного
деления, наряду с осколками, делящееся ядро испускает два или три нейтрона.
Благодаря этому становится возможным не только продолжение начавшегося деления
ядер, но и лавинообразное его нарастание (рис. 1).
Деление ядер связано с огромным выделением энергии. Так, при делении урана-235 происходит выделение около 75 млн. кДж энергии на 1 г урана. Это обусловило использование урана и плутония в качестве ядерного горючего в атомных энергетических установках и в качестве взрывчатого вещества в атомных бомбах.
Для взрыва ядерного материала необходимо такое развитие цепного процесса, при котором выделившаяся энергия достигнет взрывного порога. Это может быть обеспечено при определенной массе делящегося вещества. Минимальную массу этого вещества, необходимую для взрыва, называют критической. Однако, если два куска делящегося материала, которые в сумме составляют критическую массу, находятся на каком-то расстоянии друг от друга, то взрыва не происходит. Достаточно соединить эти куски и произойдет взрыв. После сказанного будет понятен принцип устройства атомной бомбы (рис. 2): запал 4 обеспечивает взрыв обычного взрывчатого вещества 1, это приводит в соприкосновение куски ядерного горючего 2, которые вместе составляют критическую массу, и происходит взрыв.
4. Используемая литература.
1. Петров М.М. и др. Неорганическая химия. - Л.: Химия, 1998.
2. Угай Я.А. Неорганическая химия : Учебник для хим. Спец. Вузов. – М.: Высшая школа, 1989.
3. Карапетьянц М.Х. , Дракин С.И. Общая и неорганическая химия. Учебник для вузов. – М.: Химия,1993.
4. Глинка Н.Л. Общая химия.- Л.: Химия, 1975.